��Ŀ����
����Ŀ����������Ҫ��������������ͭ�������г����Ľ�����
��1��Fe��Cu�������65%�����ᷴӦ���������NO2 �� �÷�Ӧʹ�õ���������ʵ���Ũ��Ϊmol/L����֪��=1.4g/cm3����
��2����Ϊ0.1mol��Cu��Fe�������������ijŨ�ȵ����ᷴӦ����4.48L���壨��״���£�����÷�Ӧ���ĵ�����Ϊmol��
��3��4.4gFe��Cu���������������ᷴӦ���ų����������״���µ�1.12L��������Ϻ�ͨ��ˮ��ǡ�ñ���ȫ���գ�������ͭ������Ϊg��
��4��Fe��Cu����ﹲ��a mol������ͭ�����ʵ�������ΪX�����û����ȫ��Ͷ��b mol��������ʹ���ַ�Ӧ���ٶ�����Ļ�ԭ�������NO��������Һ�н�������ֻ��Fe2+��Cu2+ʱ����b��ȡֵ��Χ������a��x��ʾ����
���𰸡�
��1��14.44
��2��0.7
��3��1.6
��4��![]() ��b��
��b�� ![]() ����x=0.2ʱ����ҺFe2+��Fe3+�����ʵ������ʱ���ڱ�״���²���NO 6.72L����a��b��ֵ����д����Ҫ�ļ�����̣�
����x=0.2ʱ����ҺFe2+��Fe3+�����ʵ������ʱ���ڱ�״���²���NO 6.72L����a��b��ֵ����д����Ҫ�ļ�����̣�
�⣺��x=0.2����Һ��Fe3+��Fe2+�����ʵ������ʱ��Cuȫ��Ϊͭ���ӣ����Բμӷ�Ӧ��CuΪ0.2amol��Fe3+��Fe2+�����ʵ�����Ϊ0.4amol��
HNO3��NO��N��3���ӣ�����6.72LNO���弴0.3mol���ܼƵ�0.9 mol���ӣ�
Cu��Cu2+ �� Cuʧ2���ӣ���ʧ0.4a mol���ӣ�
Fe��Fe2+ �� Feʧ2���ӣ���ʧ0.8amol���ӣ�
Fe��Fe3+ �� Feʧ3���ӣ���ʧ1.2amol���ӣ�
���ݵ�ʧ����������ȣ����ԣ�0.9=0.4a+0.8a+1.2a�����a=0.375mol��
���ݵ�ԭ���غ��֪��b=2n��Cu2+��+2n��Fe2+��+3n��Fe3+��+2n��NO��=2��0.2��0.375+2��0.4��0.375+3��0.4��0.375+0.3=1.2mol��
��a��ֵΪ0.375��b��ֵΪ1.2��
���������⣺��1��Fe��Cu�������65%�����ᷴӦ���������NO2 �� �÷�Ӧʹ�õ���������ʵ���Ũ��= ![]() =14.44mol/L�����Դ��ǣ�14.44����2����Ϊ0.1mol��Cu��Fe�������������ijŨ�ȵ����ᷴӦ����4.48L���壨��״���£������ʵ���n=
=14.44mol/L�����Դ��ǣ�14.44����2����Ϊ0.1mol��Cu��Fe�������������ijŨ�ȵ����ᷴӦ����4.48L���壨��״���£������ʵ���n= ![]() =0.2mol��ͭ�������������ᷴӦ����������ԭ��Ӧ�����ᱻ��ԭΪ�����������������Ϊ�����Σ�Cu��NO3��2 �� Fe��NO3��3 �� ��Ԫ���غ���㣬��÷�Ӧ���ĵ��������ʵ���=0.1mol��2+0.1mol��3+0.2mol=0.7mol�����Դ��ǣ�0.7����3��ͭ������������ᷴӦ��������ͭ�����������뵪�������������������������ˮ��Ӧ�������ᣬ�ݹ��������̣������ṩ�ĵ��ӵ���������õĵ��ӣ�n��O2��=
=0.2mol��ͭ�������������ᷴӦ����������ԭ��Ӧ�����ᱻ��ԭΪ�����������������Ϊ�����Σ�Cu��NO3��2 �� Fe��NO3��3 �� ��Ԫ���غ���㣬��÷�Ӧ���ĵ��������ʵ���=0.1mol��2+0.1mol��3+0.2mol=0.7mol�����Դ��ǣ�0.7����3��ͭ������������ᷴӦ��������ͭ�����������뵪�������������������������ˮ��Ӧ�������ᣬ�ݹ��������̣������ṩ�ĵ��ӵ���������õĵ��ӣ�n��O2��= ![]() =0.05mol�� ��Cu��Fe�����ʵ����ֱ�Ϊx��y����
=0.05mol�� ��Cu��Fe�����ʵ����ֱ�Ϊx��y����
���������з��̣�x��64g/mol+y��56g/mol=4.4g
���ݵ����غ��з��̣�2x+3��y=0.05mol��4
��ã�x=0.025mol��y=0.05mol
m��Cu��=0.025mol��64g/mol=1.6g�����Դ��ǣ�1.6����4���ٵ���Һ�еĽ�������ֻ��Fe2+��Cu2+ʱ��˵��Cuǡ����ȫ��Ӧ������ʣ�࣬��HNO3��Fe����ȫ��Ӧ�����������ʣ�࣬��Fe2+��ᱻ��һ������ΪFe3+�������Feʣ�࣬����Cu2+������Ӧ����
HNO3��NO��N��3���ӣ��豻��ԭ��HNO3Ϊy mol���ܼƵ�3y mol���ӣ�
Cu��Cu2+ �� Cuʧ2���ӣ���μӷ�Ӧ��CuΪz mol���ܼ�ʧ2z mol���ӣ�
Fe��Fe2+ �� Feʧ2���ӣ��μӷ�Ӧ��FeΪa��1��x�� mol���ܼ�ʧ2a��1��x�� mol���ӣ�
���ݵ�ʧ����������ȣ����ԣ�3y=2z+2a��1��x�� ��
��Ӧ���������õ���������Fe��NO3��2��Cu��NO3��2 �� �����������õ���������NO����NԪ���غ㣬�����У�y+2a��1��x��+2z=b ��
�������̣���ȥy��������b= ![]() ��
��
�μӷ�Ӧ��Cu�����ʵ���z��ȡֵ����0�����Ϊax��������У��ɵ� ![]() ��b��
��b�� ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ��b��
��b�� ![]() ��
��

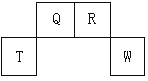
����Ŀ��������Ԫ��X,Y,Z,W��Ԫ�����ڱ������λ����ͼ��ʾ����Y������������������������ȣ���Ҫ��ش��������⣺
X | ||||
Y | Z | W |
��1��д��X��ԭ�ӽṹʾ��ͼ ��
��2���о�һ����ʵ˵��X�ǽ�����ǿ��Z�����û�ѧ����ʽ��ʾ��
��3����Y���Ȼ�������Ե�ԭ�����������ӷ���ʽ��ʾ��