题目内容
【题目】短周期元素X,Y,Z,W在元素周期表中相对位置如图所示其中Y所处的周期序数与族序数相等.按要求回答下列问题:
X | ||||
Y | Z | W |
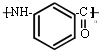
(1)写出X的原子结构示意图 .
(2)列举一个事实说明X非金属性强于Z:(用化学方程式表示)
(3)含Y的氯化物呈酸性的原因是(用离子方程式表示)
【答案】
(1)
(2)2HNO3+Na2SiO3=2NaNO3+H2SiO3↓
(3)Al3++3H2O?Al(OH)3+3H+
【解析】解:短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,Y所处的周期序数与族序数相等,短周期元素,则Y为第三周期第ⅢA族元素,即Y为Al,由元素的位置可知,Z为Si,X为N,W为S,(1)X为N元素,其原子序数为7,核外含有2个电子层,其原子结构示意图为: 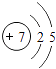 ,
,
所以答案是: 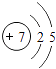 ;(2)X为N,W为S,通过最高价氧化物对应水合物的酸性强弱可以判断非金属性N大于S,反应反应为:2HNO3+Na2SiO3=2NaNO3+H2SiO3↓,
;(2)X为N,W为S,通过最高价氧化物对应水合物的酸性强弱可以判断非金属性N大于S,反应反应为:2HNO3+Na2SiO3=2NaNO3+H2SiO3↓,
所以答案是:2HNO3+Na2SiO3=2NaNO3+H2SiO3↓;(3)Y的氯化物为氯化铝,氯化铝溶液中,铝离子水解生成氢氧化铝和氢离子,溶液呈酸性,反应的离子方程式为:Al3++3H2OAl(OH)3+3H+ ,
所以答案是:Al3++3H2OAl(OH)3+3H+ .

 优加精卷系列答案
优加精卷系列答案【题目】离子方程式CO32-+2H+=H2O+CO2↑ 表示 ( )
A. 碳酸盐与盐酸之间的反应 B. 一切碳酸盐与一切酸之间的反应
C. 可溶性碳酸盐与酸之间的反应 D. 可溶性碳酸盐与强酸之间的反应
【题目】下表是元素周期表的一部分:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ | ⑩ |
针对表中的①~⑩号元素,用元素符号或化学式填空:
(1)在这些元素中,最易失电子的元素是____,非金属性最强的元素是____。
(2)化学性质最不活泼的元素是____,其原子结构示意图为__________。
(3)元素的最高价氧化物对应的水化物中呈两性的氢氧化物与氢氧化钠溶液反应的离子方程式是______________________________。
(4)在②⑤⑦⑨四种元素中,原子半径由大到小的顺序是___________________
(5)在③④⑥三种元素中,离子半径由大到小的顺序是___________________。
(6)元素⑥、⑩的最高价氧化物对应的水化物中,酸性较强的是___________________。
(7)请设计实验证明⑦原子得电子能力比⑥原子强_____________________________。