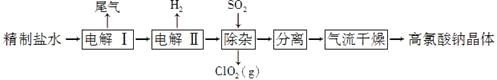
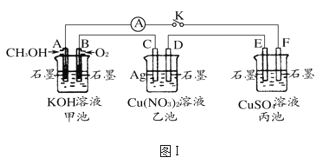
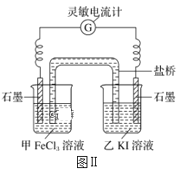
题目内容
【题目】在如图所示电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液时,则灯光由亮变暗至熄灭后又逐渐变亮的是( )
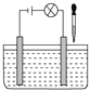
A.盐酸中逐滴加入食盐溶液
B.醋酸中逐滴加入氢氧化钠溶液
C.饱和石灰水中不断通入CO2
D.醋酸中逐滴加入氨水
【答案】C
【解析】
若向某一电解质溶液中逐滴加入另一溶液时,灯泡由亮变暗,说明溶液中电解质的浓度降低,说明所加入物质能与溶液中电解质反应生成弱电解质或沉淀,至熄灭后又逐渐变亮,说明完全反应时溶液电荷浓度接近0,当另一溶液过量时,溶液中电荷浓度逐渐增大,又逐渐变亮,以此解答。
A.盐酸溶液中逐滴加入食盐,溶液电荷浓度不为0,灯泡不可能熄灭,A错误;
B.醋酸中逐滴加入氢氧化钠溶液生成醋酸钠,溶液中存在自由移动的离子,溶液电荷浓度不为0,灯泡不可能熄灭,B错误;
C.饱和石灰水中不断通入CO2,完全反应时生成碳酸钙和水,溶液电荷浓度接近0,灯泡熄灭,符合题目要求,C正确;
D.醋酸中逐滴加入氨水,生成醋酸铵,溶液电荷浓度不为0,灯泡不可能熄灭,D错误;
故合理选项是C。

 阅读快车系列答案
阅读快车系列答案【题目】下列能用勒夏特列原理解释的事实是
A.碳酸钙不溶于水,但溶于盐酸
B.由2NO2(g)N2O4(g) 组成的平衡体系,加压后颜色加深
C.工业上选择常压条件合成SO3
D.选择450℃左右的温度合成氨
【题目】氨催化分解既可防治氨气污染,又能得到氢能源,得到广泛研究。
(1)已知:①反应I:4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) ΔH1=-1266.6 kJ·mol-1
2N2(g)+6H2O(g) ΔH1=-1266.6 kJ·mol-1
②H2(g)+![]() O2(g)=H2O(l) △H2=-285.8 kJ·mol-1
O2(g)=H2O(l) △H2=-285.8 kJ·mol-1
③H2O(l)═H2O(g) ΔH3=+44.0 kJ·mol-1
则反应2NH3(g)![]() N2(g)+3H2(g)的反应热△H=___。
N2(g)+3H2(g)的反应热△H=___。
(2)合成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g) △H2,在10 L恒容密闭容器中加入4 mol CO和8 mol H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g) △H2,在10 L恒容密闭容器中加入4 mol CO和8 mol H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时n(H2)随时间的变化如下表所示:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |

①△H2_____(填“>”“<”或“=”)0。
②下列说法正确的是_______(填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
③03min内用CH3OH表示的反应速率v(CH3OH)=___(保留三位小数)。
④200℃时,该反应的平衡常数K=__。向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡__(填“正向”、“逆向”或“不”)移动。
(3)体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2![]() 2SO3,并达到平衡,在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率(______________)
2SO3,并达到平衡,在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率(______________)
A. 等于p% B. 大于p% C. 小于p% D. 无法判断