题目内容
下列晶体属于离子晶体的是
| A.镁 | B.干冰 | C.氟化钾 | D.金刚石 |
C
解析试题分析:A、镁是金属,属于金属晶体;B、干冰是固态二氧化碳,属于分子晶体;D是原子晶体;故选C。
考点:晶体类型的判断

练习册系列答案
相关题目
下列说法正确的是
①离子化合物一定含离子键,也可能含极性键或非极性键
②同位素的性质几乎完全相同
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
| A.①③⑤ | B.②④ | C.①③ | D.②③④ |
下列说法错误的是
| A.含有共价键的化合物一定是共价化合物 |
| B.在共价化合物中一定含有共价键 |
| C.含有离子键的化合物一定是离子化合物 |
| D.双原子单质分子中的共价键一定是非极性键 |
中心原子采取sp2杂化的是 ( )
| A.NH3 | B.BCl3 | C.PCl3 | D.H2O |
下列推断正确的是 ( )
| A.BF3是三角锥形分子 |
B.NH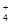 的电子式: 的电子式: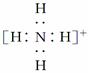 ,离子呈平面形结构 ,离子呈平面形结构 |
| C.CH4分子中的4个C—H键都是氢原子的1s轨道与碳原子的p轨道形成的sp σ键 |
| D.CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个s-sp3 σ键 |
下列有关化学键与晶体结构说法正确的是
| A.两种元素组成的分子中一定只有极性键 |
| B.离子化合物的熔点一定比共价化合物的高 |
| C.非金属元素组成的化合物一定是共价化合物 |
| D.含有阴离子的化合物一定含有阳离子 |
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
A.NH3的结构式为: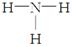 | B.乙烯的结构简式: CH2CH2 |
C.CH4分子的比例模型: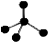 | D.-CH3(甲基)的电子式为: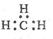 |
有关CH2=CH-C≡N分子的说法正确的是
A.3个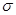 键,3个π键 键,3个π键 | B.4个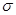 键,3个2π键 键,3个2π键 |
C.6个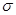 键,2个π键 键,2个π键 | D.6个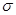 键,3个π键 键,3个π键 |
下列各项比较中前者高于(或大于或强于)后者的是
| A.CCl4和SiCl4的熔点 |
B.邻羟基苯甲醛(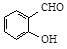 )和对羟基苯甲醛( )和对羟基苯甲醛(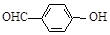 )的沸点 )的沸点 |
| C.SO2和CO2在水中的溶解度 |
| D.H2SO3和H2SO4的酸性 |