题目内容
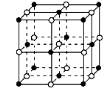
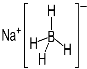
【题目】GaN、GaP、GaAs是人工合成的一系列新型半导体材料,其晶体结构均与金刚石相似。铜是重要的过渡元素,能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。回答下列问题:

(1)基态Ga原子价电子的轨道表达式为________________;
(2)熔点:GaN_____GaP(填“>”或“<”);
(3)第一电离能:As_____Se(填“>”或“<”);
(4)Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是______;
a.配位键 b.极性键 c.离子键 d.非极性键
(5)乙二胺分子中氮原子轨道的杂化类型为________,乙二胺和三甲胺[N(CH3)3]均属于胺。但乙二胺比三甲胺的沸点高很多,原因是___________;
(6)Cu的某种晶体晶胞为面心立方结构,晶胞边长为acm,铜原子的半径为rcm。该晶体中铜原子的堆积方式为_______型(填“A1”、“A2”或“A3”),该晶体密度为____g/cm3(用含a和NA的代数式表达),该晶体中铜原子的空间利用率为______(用含a和r的代数式表达)。
【答案】 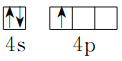 > > c sp3 乙二胺分子间可形成氢键,三甲胺分子间不能形成氢键 A1
> > c sp3 乙二胺分子间可形成氢键,三甲胺分子间不能形成氢键 A1 ![]()
![]()
【解析】(1)Ga原子是31号元素,根据构造原理写出Ga原子的电子排布式为1s22s22p63s23p63d104s24p1,价电子为4s24p1,基态Ga原子价电子的轨道表达式为![]() ;(2)GaN晶体结构与单晶硅相似,GaN属于原子晶体,N原子半径小于P,共价键键能大,熔点:GaN>GaP;(3)As的非金属性弱于Se,非金属性越强,第一电离能越大,但是由于As的p轨道电子处于半充满状态,故As的第一电离能>Se,第一电离能:As>Se;(4)铜离子提供空轨道,乙二胺中氮原子提供孤对电子形成配位键,乙二胺中两个碳形成非极性键,Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是离子键,故选C;(5)氮原子形成3个σ键和一对孤电子对,乙二胺分子中氮原子轨道的杂化类型为sp3;乙二胺分子间可形成氢键,三甲胺分子间不能形成氢键,故乙二胺比三甲胺的沸点高很多;(6)Cu的某种晶体晶胞为面心立方结构,晶胞边长为acm,铜原子的半径为rcm。该晶体中铜原子的堆积方式为A1;晶胞中Cu原子数为8×1/8+6×1/2=4,
;(2)GaN晶体结构与单晶硅相似,GaN属于原子晶体,N原子半径小于P,共价键键能大,熔点:GaN>GaP;(3)As的非金属性弱于Se,非金属性越强,第一电离能越大,但是由于As的p轨道电子处于半充满状态,故As的第一电离能>Se,第一电离能:As>Se;(4)铜离子提供空轨道,乙二胺中氮原子提供孤对电子形成配位键,乙二胺中两个碳形成非极性键,Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是离子键,故选C;(5)氮原子形成3个σ键和一对孤电子对,乙二胺分子中氮原子轨道的杂化类型为sp3;乙二胺分子间可形成氢键,三甲胺分子间不能形成氢键,故乙二胺比三甲胺的沸点高很多;(6)Cu的某种晶体晶胞为面心立方结构,晶胞边长为acm,铜原子的半径为rcm。该晶体中铜原子的堆积方式为A1;晶胞中Cu原子数为8×1/8+6×1/2=4,![]() ;晶胞中4个原子的体积为:
;晶胞中4个原子的体积为:![]() ,晶胞体积为a3,该晶体中铜原子的空间利用率为
,晶胞体积为a3,该晶体中铜原子的空间利用率为![]() 。
。