题目内容
【题目】常温下,向20 mL 0.1 mol/L的K2CO3溶液中逐滴加入0.1 mol/L的稀盐酸40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)的物质的量分数随溶液pH变化的情况如下图所示。下列说法正确的是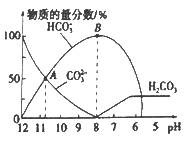
A.随着稀盐酸的加入,溶液中 ![]() 保持不变
保持不变
B.根据A点计算,Ka2 (H2CO3)的数量级为10-3
C.B 点所处的溶液中:c(K+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
D.当pH约为8时,溶液中开始放出CO2气体
【答案】A
【解析】A. 在碳酸钾的溶液中存在碳酸根的水解平衡,CO32-+H2OHCO3-+OH-,其平衡常数为Kh= ![]() ,所以随着稀盐酸的加入,只要温度不变,溶液中
,所以随着稀盐酸的加入,只要温度不变,溶液中 ![]() 保持不变,A符合题意;
保持不变,A符合题意;
B.A点pH大于10而小于11,所以c(H+)大于10-11而小于10-10,又因为此时c(CO32-)=c(HCO3-),所以Ka2 (H2CO3)= ![]() = c(H+),其数量级为10-11~10-10,A不符合题意;
= c(H+),其数量级为10-11~10-10,A不符合题意;
C. B点所处的溶液中存在电荷守恒c(K+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)+c(Cl-),所以C不符合题意;
D. 由图像可知,当pH约为8时,溶液为碳酸氢钾溶液,pH小于8以后才开始放出CO2气体,D不符合题意。
所以答案是:A
【考点精析】本题主要考查了离子积常数的相关知识点,需要掌握水的离子积Kw=c(H+)·c(OH–)=10–14(25℃)①Kw只与温度有关,温度升高,Kw增大;如:100℃ Kw=10–12②Kw适用于纯水或稀酸、稀碱、稀盐水溶液中才能正确解答此题.

 名校课堂系列答案
名校课堂系列答案【题目】下列各组物质中,满足表中图示物质在通常条件下一步转化关系的组合只有( )
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A.①②③
B.①③④
C.②③
D.①④