题目内容
【题目】X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,![]() 的最高正价与最低负价的代数和为2,下列说法正确的是( )
的最高正价与最低负价的代数和为2,下列说法正确的是( )

A.![]() 的最高价氧化物一定是酸性氧化物
的最高价氧化物一定是酸性氧化物
B.![]() 的单质是制造光导纤维的主要物质
的单质是制造光导纤维的主要物质
C.由![]() 和氢元素三种元素形成的化合物一定是共价化合物
和氢元素三种元素形成的化合物一定是共价化合物
D.X、U、W三种元素的氧化物对应的水化物酸性最强的是![]()
【答案】A
【解析】
X、Y、Z、U、W五种短周期非金属元素,![]() 的最高正价与最低负价的代数和为2,则Y为N元素,X半径大于Z,则X为C,Z为O,U的原子序数为N原子的2倍,则U为Si,W的原子序数比U大3,则W为17号元素,为Cl,据此分析解答。
的最高正价与最低负价的代数和为2,则Y为N元素,X半径大于Z,则X为C,Z为O,U的原子序数为N原子的2倍,则U为Si,W的原子序数比U大3,则W为17号元素,为Cl,据此分析解答。
由图分析可知元素 X、Y、Z、U、W分别为C、N、O、Si、Cl,
A. X为C元素,C的最高价氧化物为CO2,是酸性氧化物,故A正确;
B.制造光导纤维的主要物质是SiO2,不是Si单质,故B错误;
C.N、O和H元素形成的化合物可以是NH4NO3,由铵根离子和硝酸根离子构成,是离子化合物,故C错误;
D.C、Si、Cl元素的氧化物对应的水化物中,HClO酸性比H2CO3弱,故D错误;
答案选A。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】某同学研究金属锌与氯化铜溶液之间反应,在实验中该同学观察到的现象有:
i.产生少量气泡;ii.有红色固体生成;iii.溶液中产生白色沉淀。
为了解释上述现象,某同学查阅资料,获得如下信息:
编号 | 化学反应离子方程式 |
1 | Zn+Cu2+ |
2 | Zn+2Cu2+ |
3 | Cu++2Cl- |
4 | Cu++Cl- |
(1)请结合离子方程式解释产生少量气泡的原因:___。
(2)Zn与CuCl2反应生成白色沉淀的离子方程式是___。
(3)为了探究影响生成白色沉淀的因素,该同学进一步实验。取不同浓度CuCl2溶液,加入锌并振荡,均立刻产生少量气泡和红色固体,其他实验现象如下。
| 编号 | 浓度(rnol/L) | 试剂(锌均过量) | 实验现象 |
a | 0.5 | 锌片 | 立刻出现少量白色沉淀 | |
b | 1 | 锌片 | 立刻出现白色沉淀 | |
1 | 锌粉 | 立刻出现大量白色沉淀 | ||
d | 1 | 锌片、适量NaCl固体 | 少量白色沉淀,振荡迅速溶解 |
①对比实验a、b,实验结论是___。
②某同学从化学平衡的角度分析,d中白色沉淀溶解可能的原因是___(用离子方程式表示)。为证明该同学分析的原因正确,向b试管中加入适量___,振荡,观察到___,证明该同学分析的原因正确。
(4)利用沉淀法除去杂质在实际生产中应用广泛。
①在工业中冶炼锌,为了除去ZnSO4电解液溶液中的C1-,可加入___和___,生成沉淀而除去。
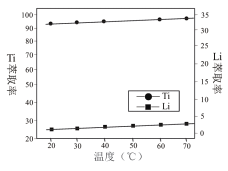
②通过进一步查阅资料得知:CuCl的形成与溶液的pH及Cu2+等离子浓度有关,一定条件下,通过实验得出pH、Cu2+浓度对Cl-沉淀的影响如图所示:

根据图,除去该电解液中Cl-的最佳条件是___。