题目内容
【题目】钛酸锂电池应用广泛, 电池放电后负极材料主要含有Li4Ti5O12、 铝箔及少量Fe, 可通过下列工艺流程回收钛、 锂。回答下列问题:

(1) Li4Ti5O12中, Ti元素的化合价为___, 滤液1中含金属的阴离子是___(填离子符号)。
(2) 酸浸时 Li4Ti5O12发生的反应是: Li4Ti5O12+7H2SO4+5H2O2=2Li2SO4+5[TiO(H2O2)]SO4+7H2O, 该反应是否属于氧化还原反应?___(填 “是” 或 “否”); 滤渣1是___。
(3) 向[TiO(H2O2)]SO4溶液中加入Na2SO3溶液发生反应的离子方程式为___。
(4) 向TiOSO4溶液中通入NH3发生反应的离子方程式为___。
(5) 沉淀TiO(OH)2用蒸馏水洗涤的目的是___。
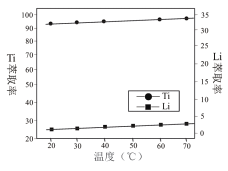
(6) 萃取时, 温度对萃取率的影响如图所示。由图分析知实验时选择在常温下进行即可, 理由是__。
(7)“萃取” 和 “反萃取” 可简单表示为:[TiO(H2O2)]2++2(HA)2![]() [TiO(H2O2)](HA2)2+2H+,则反萃取过程中加入的试剂X是___。
[TiO(H2O2)](HA2)2+2H+,则反萃取过程中加入的试剂X是___。
【答案】+4 AlO2-或Al(OH)4 - 否 Fe(OH)3 [TiO(H2O2)]2++SO32-=TiO2++SO42-+H2O TiO2++2NH3+ 2H2O=TiO(OH)2↓+2NH4+ 除去沉淀表面硫酸盐杂质 因常温下钛的萃取率已经比较高(90%以上),温度升高对萃取率的增加幅度很小,所以不必升温 H2SO4
【解析】
由流程图可知,钛酸锂电池放电后负极材料主要含有Li4Ti5O12、 铝箔及少量Fe,加入氢氧化钠溶液碱浸,铝箔溶于氢氧化钠溶液生成偏铝酸钠和氢气,其他成分不溶于碱,过滤后滤液含有偏铝酸钠溶液;碱浸后的固体加入硫酸和过氧化氢酸浸氧化,Fe转化为Fe3+,加入氢氧化钠溶液调pH生成Fe(OH)3沉淀过滤除去,酸浸时 Li4Ti5O12发生的反应是: Li4Ti5O12+7H2SO4+5H2O2=2Li2SO4+5[TiO(H2O2)]SO4+7H2O,经萃取和反萃取得到TiO(H2O2)] TiO(H2O2)SO4,水相中加入碳酸钠溶液得到Li2CO3沉淀;在TiO(H2O2)SO4溶液中加入亚硫酸钠溶液还原得到TiOSO4,再通入氨气产生TiO(O H)2沉淀,过滤后经蒸馏水洗去表面吸附的硫酸盐,再经干燥、煅烧得到纳米TiO2,据此分析解答。
(1) Li4Ti5O12中,Li为+1价,O为-2价,则 Ti元素的化合价为(12![]() 2-1
2-1![]() )
)![]() 5=+4;根据以上分析,碱浸时铝箔溶于氢氧化钠溶液生成偏铝酸钠,过滤后滤液含有偏铝酸钠溶液,所以滤液1中含金属的阴离子是AlO2-,
5=+4;根据以上分析,碱浸时铝箔溶于氢氧化钠溶液生成偏铝酸钠,过滤后滤液含有偏铝酸钠溶液,所以滤液1中含金属的阴离子是AlO2-,
因此,本题正确答案是:+4;AlO2-;
(2) 由反应方程式 Li4Ti5O12+7H2SO4+5H2O2=2Li2SO4+5[TiO(H2O2)]SO4+7H2O, 可知,反应前后元素化合价没发生变化,所以该反应不是氧化还原反应;
碱浸后的固体加入硫酸和过氧化氢酸浸氧化,Fe转化为Fe3+,加入氢氧化钠溶液调pH生成Fe(OH)3沉淀过滤除去,故滤渣1是Fe(OH)3,
因此,本题正确答案是:否;Fe(OH)3;
(3) [TiO(H2O2)]SO4与Na2SO3溶液发生氧化还原反应,反应的离子方程式为[TiO(H2O2)]2++SO32-=TiO2++SO42-+H2O,
因此,本题正确答案是:[TiO(H2O2)]2++SO32-=TiO2++SO42-+H2O;
(4) 由流程可知,TiOSO4溶液中通入NH3发生反应生成TiO(OH)2沉淀,反应的离子方程式为TiO2++2NH3+ 2H2O=TiO(OH)2↓+2NH4+,
因此,本题正确答案是:TiO2++2NH3+ 2H2O=TiO(OH)2↓+2NH4+ ;
(5) 沉淀TiO(OH)2表面会吸附溶液中的硫酸盐,所以要用蒸馏水洗涤除去杂质,
因此,本题正确答案是:除去沉淀表面硫酸盐杂质;
(6) 由温度对萃取率的影响图可知,常温下钛的萃取率已经比较高(90%以上),温度升高对萃取率的增加幅度很小,所以不必升温,实验时选择在常温下进行即可,
因此,本题正确答案是:因常温下钛的萃取率已经比较高(90%以上),温度升高对萃取率的增加幅度很小,所以不必升温;
(7) [TiO(H2O2)]2++2(HA)2![]() [TiO(H2O2)](HA2)2+2H+,根据平衡移动原理,反萃取过程是使平衡逆向移动,可以采取增大生成物浓度得方法,即增大氢离子浓度,加入的试剂X是H2SO4,
[TiO(H2O2)](HA2)2+2H+,根据平衡移动原理,反萃取过程是使平衡逆向移动,可以采取增大生成物浓度得方法,即增大氢离子浓度,加入的试剂X是H2SO4,
因此,本题正确答案是:H2SO4。

 阅读快车系列答案
阅读快车系列答案