题目内容
12.最近《美国科学院院刊》发表了关于人体体香的研究文章称:人的体味中存在两种名为“AND”和“EST”的荷尔蒙,它们的结构简式如图.结合以上信息,下列说法正确的是( )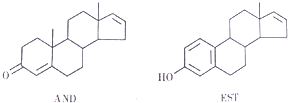
| A. | 这两种分子均能与NaOH溶液反应 | |
| B. | AND和KST分别与足量氢气加成后的两种产物互为同系 | |
| C. | AMD和EST均瓸于芳香族化合物 | |
| D. | EST的M分丼构体中,有的结构中含有葱环(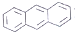 ) ) |
分析 A.这两种物质中都含有碳碳双键,但AND中含有羰基、EST中含有苯环和酚羟基;
B.结构相似,分子组成上相差1个或者若干个CH2基团的化合物互称为同系物;
C.AND中不含苯环;
D.EST的同分异构体中其不饱和度为8,蒽环的不饱和度是10.
解答 解:A.这两种物质中都含有碳碳双键,但AND中含有羰基、EST中含有苯环和酚羟基,所以AND不和NaOH反应,EST和NaOH反应,故A错误;
B.与足量H2反应后产物相差一个CH2基团,互为同系物,故B正确;
C.AND中不含苯环,所以不是芳香族化合物,故C错误;
D.EST的同分异构体中其不饱和度为8,蒽环的不饱和度是10,所以EST的同分异构体中有的结构中不可能含有蒽环,故D错误;
故选B.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系是解本题关键,同时还考查基本概念,易错选项是D.

练习册系列答案
相关题目
2.辽宁舰航母入列到中国海军极大提升了中国的军心、民心,我国的国防从此又多了一把利器.
(1)航母升降机可由铝合金制造.
①铝合金硬度较纯铝的硬度大(填“大”或“小”).工业炼铝的原料由铝土矿提取而得,写出电解氧化铝炼铝的化学方程式2Al2O3 $\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑.
②Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,焊接过程汇总使用的保护气为Ar(填化学式).
(2)航母舰体为合金钢.
①舰体在海水中发生的电化学腐蚀的类型主要为吸氧腐蚀,写出此类腐蚀的正极反应式O2+4e-+2H2O=4OH-.
②舰母用钢由生铁冶炼而成,在炼钢过程中为降低生铁中碳的含量需加入的物质为氧气(或氧化亚铁等).
(3)舰母螺旋桨主要用铜合金制造.
①80.0Cu•Al合金用酸完全溶解后,加入过量氨水,过滤得白色沉淀39.0g,则合金中Cu的质量分数为83.1%(保留一位小数).
②某些金属离子形成氢氧化物沉淀的Ph如下表所示,为分析某铜合金的成分,用酸 将其完全溶解后,用NaOH溶液调pH.当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀,结合表中信息推断该合金中除铜外一定含有Al、Ni.
(1)航母升降机可由铝合金制造.
①铝合金硬度较纯铝的硬度大(填“大”或“小”).工业炼铝的原料由铝土矿提取而得,写出电解氧化铝炼铝的化学方程式2Al2O3 $\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑.
②Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,焊接过程汇总使用的保护气为Ar(填化学式).
(2)航母舰体为合金钢.
①舰体在海水中发生的电化学腐蚀的类型主要为吸氧腐蚀,写出此类腐蚀的正极反应式O2+4e-+2H2O=4OH-.
②舰母用钢由生铁冶炼而成,在炼钢过程中为降低生铁中碳的含量需加入的物质为氧气(或氧化亚铁等).
(3)舰母螺旋桨主要用铜合金制造.
①80.0Cu•Al合金用酸完全溶解后,加入过量氨水,过滤得白色沉淀39.0g,则合金中Cu的质量分数为83.1%(保留一位小数).
②某些金属离子形成氢氧化物沉淀的Ph如下表所示,为分析某铜合金的成分,用酸 将其完全溶解后,用NaOH溶液调pH.当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀,结合表中信息推断该合金中除铜外一定含有Al、Ni.
| 金属离子 | Fe2+ | Fe3+ | Al3- | Mg2+ | Ni2+ |
| 开始沉淀的pH值 | 6.5 | 1.6 | 3.4 | 9.4 | 7.2 |
| 完全沉淀的pH值 | 9.7 | 3.2 | 5.4 | 12.4 | 9.3 |
3.下列实验结论不正确的是( )
| 实验操作 | 现象 | 结论 | |
| A | 将石蜡油加强热(裂解)所产生的气体通入酸性高锰酸钾溶液中 | 溶液褪色 | 产物不都是烷烃 |
| B | 向盛有3mL鸡蛋清溶液的试管里,滴入几滴浓硝酸 | 鸡蛋清变黄色 | 蛋白质可以发生颜色反应 |
| C | 将碘酒滴到新切开的土豆片上 | 土豆片变蓝 | 淀粉遇碘元素变蓝 |
| D | 将新制Cu(OH)2与葡萄糖溶液混合加热 | 产生红色沉淀 | 葡萄糖具有还原性 |
| A. | A | B. | B | C. | C | D. | D、 |
20.下列实验装置及描述正确的是( )
| A. |  该图装置不能这么碳酸与苯酚的酸性强弱 | |
| B. | 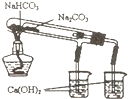 该图可验证NaHCO3和Na2CO3的热稳定性 | |
| C. | 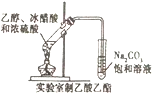 实验室可用该装置制取少量的乙酸乙酯 | |
| D. | 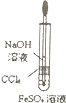 该图装置可用于制备Fe(OH)2 |
17.下列反应的离子方程式书写正确的是( )
| A. | 过量HI溶液加入到Fe(NO3)3溶液中:2Fe3++2I-═2Fe2++I2 | |
| B. | 含等物质的量的MgCl2、Ba(OH)2、HNO3三种溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| C. | CaCO3溶于醋酸:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+2H2O | |
| D. | 向海带灰浸出液中加入硫酸、双氧水:2I-+H2O2═2OH-+I2 |
4.已知某酸H2B在水溶液中存在下列关系::①H2B?H++HB-,②HB-?H++B2-.则下列关于酸式盐NaHB的溶液
的说法中一定正确的是( )
的说法中一定正确的是( )
| A. | NaHB的电离方程式为:NaHB?Na-+H-+B2- | |
| B. | NaHB溶液一定呈酸性 | |
| C. | NaHB和NaOH溶液反应的离子方程式为H++OH-═H20 | |
| D. | NaHB溶液中一定存在:c(Na+)+c(H+)═c(HB-)+2c(B2-)+c(OH-) |
11.NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温下,78g Na202中含有的阴离子数为2NA | |
| B. | 常温下,1L 0.1 mol/L NH4NO3溶液中含有的NH4 +数为0.1NA | |
| C. | 标准状况下,22.4 L己烷中含有的共价键的数目为19 NA | |
| D. | 30 g SiO2晶体中含有Si-O键的数目为2 Na |
 将纯锌片和纯铜片按如图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
将纯锌片和纯铜片按如图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题: