��Ŀ����
����Ŀ�����ںͽ�������ᣬ����Դ�Ͳ��ϵ�������Խ��Խ������ѧϰ��ѧ��Ϊ����ʶ���ʣ��������ʣ���������Դ����չ�������δ�������������й���Դ�����⣺
��1��δ������Դ���ص�����Դ�ḻ����ʹ��ʱ�Ի�������Ⱦ����Ⱦ��С���ҿ�����������������δ������Դ�����ǣ�________
����Ȼ����ú��������ʯ����̫��������������������������
A���٢ڢۢ� B���ݢޢߢ� C���ۢݢޢߢ� D���ۢܢݢޢߢ�
��2���˶�����ʹ�õĻ���ȼ��һ���DZ���(C3H8)����������������Ŀ��
����֪11g����(C3H8)��298K��101Kpa��������ȫȼ������CO2��Һ̬ˮʱ�ų�������Ϊ555kJ����д������ȼ���ȵ��Ȼ�ѧ����ʽ��_____________��
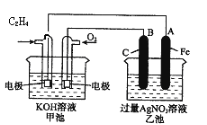
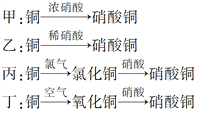
���Ա���(C3H8)�Ϳ���Ϊԭ�ϣ�ϡ����Ϊ�������Һ_____________(���ܻ���)��Ƴɳأ�
���ܣ���д��ͨ�����(C3H8)����һ��Ϊ��_____________����������_____________��������Ӧ��
�����ܣ��������ǣ�_____________��
��������һ�������·������ⷴӦ���Եõ���ϩ��
��֪��C3H8(g)��CH4(g)��HC��CH(g)��H2(g)��H1=+156.6kJ��mol��1
CH3CH=CH2(g)��CH4(g)��HC��CH(g)��H2=+32.4kJ��mol��1
����ͬ�����£���ӦC3H8(g)��CH3CH=CH2(g)��H2(g)����H=_______
��3����֪��H��H���ļ���Ϊ436KJ/mol��H��N���ļ���Ϊ391KJ/mol�����ݻ�ѧ����ʽ��N2+3H2![]() 2NH3��H=-92.4KJ/mol��
2NH3��H=-92.4KJ/mol��
��������N��N���ļ���Ϊ_______________��
�������������Ȼ�ѧ����ʽ��ͬ�¶Ⱥ����һ���������У�ͨ��1molN2��3molH2����ַ�Ӧ�ָ�ԭ�¶�ʱ�ų�������_______________92.4KJ(����ڻ�С�ڻ����)��
���𰸡�
��1��C��
��2����C3H8(g)��5O2(g)=3CO2(g)��4H2O(l)��H=��2220kJ��mol��1��
���ܣ�������������H=124.2kJ��mol��1
��3����945.6KJ/mol����С�ڡ�
��������
�����������1��ú��ʯ�͡���Ȼ���ǻ�ʯ��Դ����������Դ����������Դ�У�̫���ܡ����ܡ������ܡ���ϫ�ܡ����ܡ����ܡ��������ܵ�����ѡC��
��2����11g��������ʵ���Ϊ��![]() =0.25mol����1mol������ȫȼ�շų�������Ϊ��55kJ ��
=0.25mol����1mol������ȫȼ�շų�������Ϊ��55kJ �� ![]() = 2220kJ�������ȼ�յ��Ȼ�ѧ����ʽΪ��C3H8(g) + 5O2(g) = 3CO2(g)+4H2O(l) ��H=-2220 kJmol-1��
= 2220kJ�������ȼ�յ��Ȼ�ѧ����ʽΪ��C3H8(g) + 5O2(g) = 3CO2(g)+4H2O(l) ��H=-2220 kJmol-1��
��ȼ�ϵ���У�������ȼ��C3H8�����ʧ���ӷ���������Ӧ���������������õ��ӷ�����ԭ��Ӧ�������缫��ӦʽΪC3H8-20e-+10CO32-=13CO2+4H2O��������ӦʽΪ��O2+2CO2+4e-=2CO32-���������ط�ӦʽΪC3H8+5O2�T3CO2+4H2O���ŵ�ʱ����������������ƶ���������������෴����̼����������ƶ����ʴ�Ϊ���ܣ���������
����֪����C3H8(g)�TCH4(g)+HC��CH(g)+H2(g) ��H1=156.6kJmol-1��
��CH3CH=CH2(g)�TCH4(g)+HC��CH(g) ��H2=32.4kJmol-1��
���ݸ�˹���ɣ���-����C3H8(g)�TCH3CH=CH2(g)+H2(g)����������H=��H1-��H2=156.6kJmol-1-32.4kJmol-1=124.2kJmol-1���ʴ�Ϊ��124.2kJmol-1��
��3������֪��H-H����Ϊ436kJ/mol��H-N����Ϊ391kJ/mol����N��N�ļ���Ϊx�����ڷ�ӦN2(g)+3H2(g)=2NH3(g)��H=-92.4kJ/mol����Ӧ��=��Ӧ����ܼ���-��������ܼ��ܣ���x+3��436kJ/mol-2��3��391kJ/mol=-92.4kJ/mol����ã�x=945.6kJ/mol���ʴ�Ϊ��945.6kJ/mol��
��N2��H2�ķ�Ӧ���ڿ��淴Ӧ��������ȫ���У����1molN2��3molH2����ַ�Ӧ�ָ�ԭ�¶�ʱ�ų�������С��92.4KJ���ʴ�Ϊ��С�ڡ�

 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�