题目内容
【题目】如图是一个化学过程的示意图。
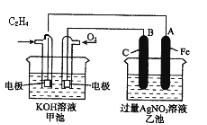
请根据该示意图完成下列题目:
(1)请问:甲池是________装置,乙池是________装置。
(2)在甲池中:通入C2H4的电极名称是___________,通入O2的电极的电极反应式是________。甲池中发生的反应的化学方程式为:________。
(3)在乙池中:B(石墨)电极的名称是________,A(Fe)电极的电极反应式为________。
(4)乙池中反应的化学方程式为________。
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2________mL(标准状况下)
【答案】
(1)原电池(或化学能转变为电能);电解池(或电能转变为化学能);
(2)负极;O2+2H2O+4e-=4OH-;C2H4+3O2=2CO2+2H2O和CO2+2KOH=K2CO3+H2O;或C2H4+3O2+4KOH=2K2CO3+4H2O。
(3)阳极;Ag++e-=Ag;
(4)4AgNO3+2H2O4Ag+O2↑+4HNO3;
(5)280。
【解析】
试题分析:(1)根据示意图,甲池是原电池装置,乙池是电解池,故答案为:原电池;电解池;
(2)在甲池中:通入C2H4的电极为负极,C2H4失去电子反应生成碳酸根离子和水,通入O2的电极为正极,正极的电极反应式为O2+2H2O+4e-=4OH-,甲池中发生的反应的化学方程式为C2H4+3O2+4KOH=2K2CO3+4H2O,故答案为:负极;O2+2H2O+4e-=4OH-;C2H4+3O2+4KOH=2K2CO3+4H2O;
(3)在乙池中:B(石墨)与燃料电池的正极相连,为阳极,则A(Fe)电极为阴极,阴极上溶液中的Ag+放电,电极反应式为Ag++e-=Ag,故答案为:阳极;Ag++e-=Ag;
(4)电解硝酸银溶液的反应的化学方程式为4AgNO3+2H2O4Ag+O2↑+4HNO3,故答案为:4AgNO3+2H2O4Ag+O2↑+4HNO3;
(5)5.40g银的物质的量为![]() =0.05mol,转移电子0.05mol,根据得失电子守恒,甲池中理论上消耗O2的物质的量为
=0.05mol,转移电子0.05mol,根据得失电子守恒,甲池中理论上消耗O2的物质的量为![]() =0.0125mol,标准状况下的体积为0.0125mol×22.4L/mol=0.28L=280mL,故答案为:280。
=0.0125mol,标准状况下的体积为0.0125mol×22.4L/mol=0.28L=280mL,故答案为:280。