题目内容
【题目】实验室模拟合成氨和氨催化氧化的流程如下:

已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
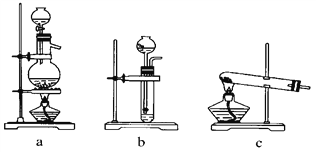
(1)从如图中选择制取气体的合适装置:氮气________、氢气________。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有________、________。
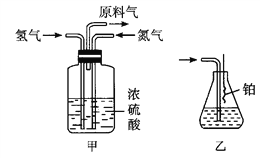
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨,________(“会”或“不会”)发生倒吸,原因是_________________。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是________,锥形瓶中还可观察到的现象是____________________________。
(5)写出乙装置中氨氧化的化学方程式:_____________________________________________。
(6)反应结束后锥形瓶内的溶液含有H+、OH-、______、________离子。
【答案】 a b 干燥气体 控制氢气和氮气的流速的作用 不会 混合气体中含有大量难溶于水的氮气 、氢气两种气体 氨的氧化反应是一个放热反应 有红棕色气体产生 4NH3+5O2![]() 4NO+6H2O NH
4NO+6H2O NH![]() NO
NO![]()
【解析】本题考查气体的制备和氨气的性质,(1)氮气实验室用饱和亚硝酸钠和饱和氯化铵溶液共热来制备,因此制取氮气的装置为a,氢气实验室用活泼金属与稀盐酸或稀硫酸来制备,不需要加热,因此制取氢气的装置为b;(2)浓硫酸具有吸收性,干燥气体,因此装置甲作用是干燥气体,合成氨的反应是可逆反应,让原料达到最大利用,应按照反应方程式中化学计量数之比通入,因此浓硫酸的另一个作用通过观察气泡,控制氢气和氮气的流速;(3)在装置乙中反应的气体中,有大量难溶于水的N2和H2,不会造成压强突然减小,引起倒吸;(4)此反应是NH3的催化氧化,铂丝保持红热,说明氨的催化氧化是放热反应,氨气催化氧化的反应方程式为:4NH3+5O2![]() 4NO+6H2O,锥形瓶上方有空气,NO与氧气反应生成NO2,因此现象是有红棕色气体产生;(5)氨气的催化氧化,氨气被氧化成NO,其反应方程式为:4NH3+5O2
4NO+6H2O,锥形瓶上方有空气,NO与氧气反应生成NO2,因此现象是有红棕色气体产生;(5)氨气的催化氧化,氨气被氧化成NO,其反应方程式为:4NH3+5O2![]() 4NO+6H2O;(6)根据问题(4)的实验现象,有NO2产生,3NO2+H2O=2HNO3+NO,氨气与生成HNO3反应,生成硝酸铵,因此溶液中含有NH4+、NO3-。
4NO+6H2O;(6)根据问题(4)的实验现象,有NO2产生,3NO2+H2O=2HNO3+NO,氨气与生成HNO3反应,生成硝酸铵,因此溶液中含有NH4+、NO3-。