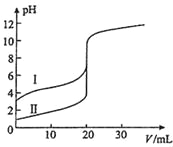
题目内容
【题目】NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
Ⅰ.(1)实验室用金属铜和稀硝酸制取NO的离子方程式为
___________________________________________________。
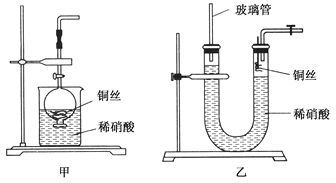
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填选项编号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是____________________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反就开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是___________________________________。
②让反应停止的操作方法及原因是________________________。
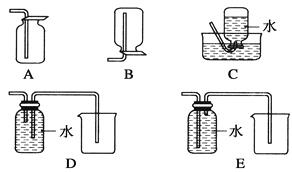
(4)以下收集NO气体的装置,合理的是________(填选项代号)。
(5)假设实验中12.8 g Cu全部溶解,需要通入标况下________mL O2才能使NO全部溶于水。
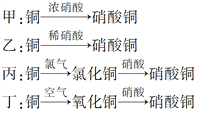
Ⅱ.用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________(填“甲”、“乙”、“丙”或“丁”),理由是___________________________________________。
【答案】 3Cu+8H++2NO![]() ===3Cu2++4H2O+2NO↑ C、D 2NO+O2===2NO2 接收被气体压出U形管的液体,防止稀硝酸溢出 关闭U形管右端导气管上的活塞,反应产生的气体将U形管右端内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止 C、D 2240m L 丁 制取相同质量的Cu(NO3)2,丁所消耗的HNO3的量最少(原料的利用率最高)且不产生污染环境的气体
===3Cu2++4H2O+2NO↑ C、D 2NO+O2===2NO2 接收被气体压出U形管的液体,防止稀硝酸溢出 关闭U形管右端导气管上的活塞,反应产生的气体将U形管右端内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止 C、D 2240m L 丁 制取相同质量的Cu(NO3)2,丁所消耗的HNO3的量最少(原料的利用率最高)且不产生污染环境的气体
【解析】I.本题考查实验方案设计的评价,(1)利用稀硝酸强氧化性,与铜发生反应,离子反应方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;(2)①所用物质不能稀硝酸反应,干扰铜和稀硝酸的反应,Fe、Al都与稀硝酸反应,Pt、玻璃不用稀硝酸反应,即C和D选项正确;②分液漏斗中含有空气,NO与氧气反应生成NO2,即2NO+O2=2NO2;(3)①关闭活塞,铜丝与硝酸反应,气体增多,压强增大,会把硝酸压入到玻璃管中,防止稀硝酸溢出;②关闭活塞,,反应产生的气体将U形管右端内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止 ; (4)因为NO与空气中氧气反应,因此收集NO用排水法收集,排水法收集气体应是短管进气长管出水,因此选项C和D正确;(5)NO与氧气的反应:4NO+3O2+2H2O=4HNO3 ,铜失去电子,最终让氧气得到,根据得失电子数目守恒,即12.8×2/64=V(O2)×4/22.4,解得V(O2)=2.24L,合2240ml;II.甲、铜与浓硝酸反应产生对环境有污染的氮的氧化物,故甲错误;乙、产生NO,污染空气,故乙错误;丙、使用氯气,氯气有毒,污染空气,故丙错误;丁、对环境无污染,故丁正确。