题目内容
【题目】元素周期表是学习物质结构与性质的重要工具。下表是元素周期表的一部分,表中所列字母a、b、c、d、e、f、g、m、n、o、r分别代表某一种元素。请回答下列问题。
a | |||||||||||||||||
c | b | n | |||||||||||||||
d | e | o | f | ||||||||||||||
m | r | g | |||||||||||||||
(1)g元素的原子序数为 ;上述所给11种元素中非金属元素共有 种。
(2)m元素在元素周期表中的位置 ;e、n二元素形成的稳定化合物的化学式为 。
(3)o元素离子的电子式为 ;化合物ba3的结构式为 。
(4)用电子式表示化合物d2n的形成过程 ;
(5)d的最高价氧化物的水化物与e的最高价氧化物反应的离子方程式 。
(6)单质r与b的最高价氧化物的水化物的稀溶液反应的离子方程式 。
【答案】(1)33、7;(2)第四周期ⅡA族、Al2O3;(3)![]() 、
、![]() (4)
(4)![]() ;(5)2OH— + Al2O3= 2AlO2—+H2O;6)3Cu+8H++2NO3— = 3Cu2++2NO↑+4H2O。
;(5)2OH— + Al2O3= 2AlO2—+H2O;6)3Cu+8H++2NO3— = 3Cu2++2NO↑+4H2O。
【解析】试题分析:(1)根据元素周期表,b为N,则g的原子序数为7+8+18=33,所给的非金属共有7种;(2)m在周期表的位置位于第四周期IIA族,e为Al,n为O,形成稳定的氧化物为Al2O3;(3)O为S,其离子带有2个单位的负电荷,离子为S2-,电子式为![]() ,b为N,a为H,ba3为NH3,结构式为:
,b为N,a为H,ba3为NH3,结构式为:![]() ;(4)d为Na,d2n为Na2O,属于离子化合物,电子式表示形成过程:
;(4)d为Na,d2n为Na2O,属于离子化合物,电子式表示形成过程:![]() ;(5)Na的最高价氧化物对应水化物为NaOH,e的最高价氧化物为Al2O3,Al2O3为两性氧化物,其离子反应方程式为:Al2O3+2OH-=2AlO2-+H2O;(6)r为铜,铜和硝酸的反应离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
;(5)Na的最高价氧化物对应水化物为NaOH,e的最高价氧化物为Al2O3,Al2O3为两性氧化物,其离子反应方程式为:Al2O3+2OH-=2AlO2-+H2O;(6)r为铜,铜和硝酸的反应离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。

【题目】中和热的测定是高中重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
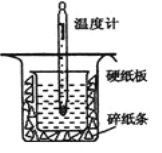
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________,除此之外,装置中的一个明显错误是 。
(2)若改用60mL 0.25mol·L-1 H2SO4和50mL 0.55mol·L-1NaOH溶液进行反应与上述实验相比,所放出的热量________ ___(填“相等”、“不相等”),若实验操作均正确,则所求中和热________ ___(填“相等”“不相等”)。
(3)实验数据如下表:
①请填写下表中的空白:
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
|
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH=______ ____ ( 取小数点后一位)。