题目内容
【题目】设NA是阿伏加德罗常数的值。下列说法正确的是( )
A. 1mol乙酸乙酯在稀硫酸中水解生成的乙醇分子中含共价键数目为8NA
B. 18.0g葡萄糖和果糖的混合物中含羟基数目为0.5NA
C. 1L0.5mol·L-1 CuSO4溶液清除P4完全反应生成Cu、H2SO4和H3PO4时转移电子数为2.5NA
D. 标准状况下,2.24LD2和H2的混合气体中含中子数目为0.2NA
【答案】B
【解析】
A.乙酸乙酯在稀硫酸中水解是可逆反应,无法计算生成乙醇的物质的量,故A错误;B.葡萄糖和果糖的分子式为C6H12O6,18.0g葡萄糖和果糖的混合物的物质的量为0.1mol, 葡萄糖和果糖的结构中均含有5个羟基,所以18.0g葡萄糖和果糖的混合物中含羟基数目为0.5NA,故B正确;C. 由CuSO4![]()
![]() 2e-,所以1L0.5mol·L-1 CuSO4溶液完全反应生成
2e-,所以1L0.5mol·L-1 CuSO4溶液完全反应生成![]() 转移的电子数为NA,故C错误;D.2H(即D)含有一个中子,1H中不含有中子,所以标准状况下,2.24L D2和H2的混合气体中含中子数目小于0.2NA,故D错误;答案:B。
转移的电子数为NA,故C错误;D.2H(即D)含有一个中子,1H中不含有中子,所以标准状况下,2.24L D2和H2的混合气体中含中子数目小于0.2NA,故D错误;答案:B。

【题目】(1)已知H—H键键能(化学键断裂时吸收或形成时释放的能量)为436 kJ/mol,N—H键键能为391 kJ/mol,根据热化学方程式:N2(g)+3H2(g)===2NH3(g) ΔH=-92.4 kJ/mol,可知![]() 键的键能是______________kJ/mol
键的键能是______________kJ/mol
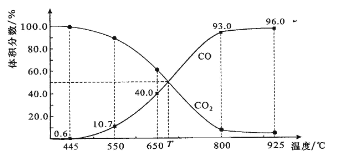
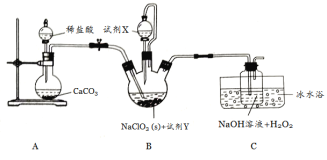
(2)碳(s)在氧气供应不充足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应:C(s)+![]() O2(g)===CO(g)的ΔH。但可设计实验、利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有________
O2(g)===CO(g)的ΔH。但可设计实验、利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有________
(3)运动会中的火炬一般采用丙烷(C3H8)为燃料。丙烷热值较高,污染较小,是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,图中的括号内应填入___(“+”或“-”)。
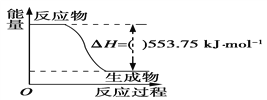
②写出表示丙烷燃烧热的热化学方程式:________________。
(4)高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
由以上表格中数据判断以下说法不正确的是__________。
A.在冰醋酸中这四种酸都没有完全电离
B.在冰醋酸中高氯酸是这四种酸中酸性最强的酸
C.在冰醋酸中硫酸的电离方程式为: H2SO4 = 2H++S![]()
D.水对这四种酸的强弱没有区分能力,但冰醋酸可以区分这四种酸的强弱
(5)常温下,0.1 mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数值变大的是________。
A.c(H+) B.![]() C.c(CH3COO-) D.c(CH3COOH)
C.c(CH3COO-) D.c(CH3COOH)