题目内容
9.下列含有羟基的化合物的水溶液显中性的是( )| A. | HONO2 | B. | HOCH3 | C. | KOH | D. | CH3COOH |
分析 含有羟基的化合物的水溶液显中性,说明该物质是非电解质,在水溶液中以分子存在,不易电离出氢离子而使溶液呈酸性,据此分析解答.
解答 解:A.硝酸中含有羟基,但羟基受硝基影响而易电离出氢离子而使溶液呈酸性,故A不选;
B.甲醇属于非电解质,在水溶液中以分子存在,不易电离,所以水溶液呈中性,故B选;
C.KOH中不含羟基,且KOH是强电解质,在水溶液中电离出氢氧根离子而使溶液呈碱性,故C不选;
D.乙酸中含有羟基,但羟基受CH3CO-的影响而易电离出氢离子而使其溶液呈酸性,故D不选;
故选B.
点评 本题考查物质水溶液酸碱性判断,明确溶质的性质是解本题关键,酸或碱或含有弱离子的盐电离或水解生成的氢离子或氢氧根离子而导致溶液呈酸碱性,易错选项是C.

练习册系列答案
相关题目
20.下列关于反应 4Li+2SOC12═4LiCl+S+SO2↑的叙述中,不正确的是( )
| A. | SOCl2是氧化剂,Li是还原剂 | |
| B. | 2 mol SOCl2参加反应,共转移4 mol电子 | |
| C. | 若将该反应设计成原电池,SOCl2在正极发生反应 | |
| D. | 若将该反应设计成原电池,可用稀硫酸作电解质溶液 |
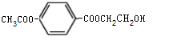
17.有机物 与氯气发生取代反应,生成的一氯代物有( )
与氯气发生取代反应,生成的一氯代物有( )
 与氯气发生取代反应,生成的一氯代物有( )
与氯气发生取代反应,生成的一氯代物有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
4.一定温度下,可逆反应A(气)+3B(气)?2C(气)在一定容积的密闭容器中进行,达到平衡的标志是( )
| A. | 混合气体的密度不再变化 | B. | A、B、C的浓度相等 | ||
| C. | 混合气体的压强不再变化 |
14.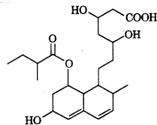 普伐他汀是一种调节血脂的药物,其结构简式如图所示.下列关于普伐他汀的描述错误的是( )
普伐他汀是一种调节血脂的药物,其结构简式如图所示.下列关于普伐他汀的描述错误的是( )
 普伐他汀是一种调节血脂的药物,其结构简式如图所示.下列关于普伐他汀的描述错误的是( )
普伐他汀是一种调节血脂的药物,其结构简式如图所示.下列关于普伐他汀的描述错误的是( )| A. | 分子中含有四种官能团 | |
| B. | 1 mol该物质最多可与3 mol NaOH反应 | |
| C. | 能发生加成反应、取代反应、水解反应 | |
| D. | 1 mol该物质最多可与2 mol H2发生加成反应 |
1.关于烷烃的叙述不正确的是( )
| A. | 分子式符合CnH2n+2的烃一定是烷烃 | |
| B. | 烷烃均能与氯水发生取代反应 | |
| C. | 辛烷的熔沸点比壬烷低 | |
| D. | 烷烃不能被酸性高锰酸钾等强氧化剂氧化 |
18. 25℃时,用0.30mol•L-1 NaOH溶液逐滴加入到10mL 0.30mol•L-1某二元酸H2R溶液,测得滴加过程中溶液pH随NaOH溶液体积变化曲线如图所示,下列说法或关系正确的是( )
25℃时,用0.30mol•L-1 NaOH溶液逐滴加入到10mL 0.30mol•L-1某二元酸H2R溶液,测得滴加过程中溶液pH随NaOH溶液体积变化曲线如图所示,下列说法或关系正确的是( )
 25℃时,用0.30mol•L-1 NaOH溶液逐滴加入到10mL 0.30mol•L-1某二元酸H2R溶液,测得滴加过程中溶液pH随NaOH溶液体积变化曲线如图所示,下列说法或关系正确的是( )
25℃时,用0.30mol•L-1 NaOH溶液逐滴加入到10mL 0.30mol•L-1某二元酸H2R溶液,测得滴加过程中溶液pH随NaOH溶液体积变化曲线如图所示,下列说法或关系正确的是( )| A. | H2R是弱酸且HR-的电离常数Ka小于它的水解常数Kb | |
| B. | 点②溶液中c(HR-)为点①溶液中c(HR-)的2倍 | |
| C. | 点③所示溶液中:c(H2R)+c(HR-)+c(R2-)=0.10mol•L-1 | |
| D. | 点④所示溶液中:c(HR-)+2c(R2-)+c(OH-)-c(H+)=0.2mol•L-1 |

 .
. .
. 、
、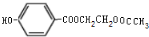 .
. .
.