题目内容
13.25℃时,KNO3在水中的饱和溶液物质的量浓度是6mol•L-1,若将1mol固体KNO3置于1L水中,则KNO3变成盐溶液过程的△H-T△S的取值为( )| A. | 小于0 | B. | 等于0 | C. | 大于0 | D. | 不能确定 |
分析 反应能否自发进行,决定于△H-T△S的大小,△H-T△S<0时反应能自发进行,△H-T△S>0时,反应不能自发进行,据此分析.
解答 解:本题中KNO3在水中的饱和溶液物质的量浓度是6mol•L-1,说明1L溶液中最多可以溶解6moLKNO3固体,所以将1mol固体KNO3置于1L水中,则完全溶解,该过程为自发过程,所以△H-T△S<0,故选:A.
点评 本题考查反应能否自发进行的条件,△H-T△S的大小决定反应能否自发进行,题目难度不大.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
4.相同物质的量的 Na+、OH-、F- 离子具有相同的( )
| A. | 质量 | B. | 质子数 | C. | 电子数 | D. | 中子数 |
1.下列反应与酸性氧化物的通性无关的是( )
| A. | 实验室用碱石灰吸收SO2 | B. | CO2与澄清石灰水作用 | ||
| C. | N2O5与水反应制备HNO3 | D. | Na2O2与水反应制备氧气 |
8.下列离子方程式书写正确的是( )
| A. | 硫酸铜溶液与氢氧化钡溶液混合:Cu2++2 OH-=Cu(OH)2↓ | |
| B. | 用小苏打(NaHCO3)治疗胃酸(主要成分是盐酸)过多:CO32-+H+═CO2↑+H2O | |
| C. | 将少量二氧化碳气体通入澄清石灰水中:2OH-+CO2═CO32-+H2O | |
| D. | 稀硫酸与氢氧化钡溶液混合:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓ |
18.氨与重水(D2O)形成的碱与盐酸反应,这一反应生成的盐中阳离子的化学式是( )
| A. | NH3D+ | B. | NH2D2+ | C. | ND3H+ | D. | NH4+ |
5.下列仪器中,能在酒精灯火焰上直接加热的玻璃仪器是( )
| A. | 试管 | B. | 蒸发皿 | C. | 烧杯 | D. | 蒸馏烧瓶 |
3.已知弱酸的电离平衡常数如下表:下列选项正确的是( )
| 弱酸 | H2CO3 | 水杨酸( ) ) |
| 电离平衡常数(925℃) | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=1.3×10-3 Ka2=1.1×10-11 |
| A. | 常温下,等浓度、等体积的NaHCO3溶液pH小于 溶液pH 溶液pH | |
| B. | 常温下,等浓度、等体积的Na2CO3溶液和  溶液中所含离子总数前者小于后者 溶液中所含离子总数前者小于后者 | |
| C. | 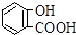 +2NaHCO3→ +2NaHCO3→ +2H2O+2CO2↑ +2H2O+2CO2↑ | |
| D. | 水杨酸的第二级电离 Ka2 远小于第一级电离Ka1的原因之一是能形成分子内氢键 |
 化学反应与能量有着密不可分的关系,回答下列问题.
化学反应与能量有着密不可分的关系,回答下列问题.