题目内容
【题目】将0.20 mol/L的盐酸和物质的量浓度为c mol/L的NaOH溶液按不同体积比配制成两种溶液。下表是配制时所取盐酸与 NaOH 溶液体积与混合后溶液中Na+与Cl-的物质的量浓度数据(忽略溶液体积变化):
溶液 | 混合前所取溶液体积(mL) | 混合后离子浓度(mol/L) | ||
HCl | NaOH | Na+ | Cl- | |
① | 30 | x | 1.5z | z |
② | 10 | y | z | 2z |
下列说法正确( )
A.x=90B.y=30C.z=0.10D.c=0.10
【答案】AD
【解析】
由题可知,混合后溶液中Na+离子全部来源于NaOH,Cl-离子全部来源于HCl,根据元素守恒列出溶液①和溶液②混合后Na+离子和Cl-离子浓度的计算式,从而进行计算。
由题可知,混合后溶液中Na+离子全部来源于NaOH,Cl-离子全部来源于HCl,则:
溶液①混合后溶液中c(Na+)=![]() =1.5zmol/L,c(Cl-)=
=1.5zmol/L,c(Cl-)=![]() =zmol/L;
=zmol/L;
溶液②混合后溶液中c(Na+)=![]() =zmol/L,c(Cl-)=
=zmol/L,c(Cl-)=![]() =2zmol/L;
=2zmol/L;
解得:x=90,c=0.10,y=10,z=0.05;
故答案选AD。

 应用题作业本系列答案
应用题作业本系列答案【题目】在测定硫酸铜晶体中结晶水含量的实验操作中:
(1)加热前应将晶体放在__________中研碎,加热是放在__________中进行,加热失水后,应放在__________中冷却。
(2)判断是否完全失水的方法是______________________________________________。
(3)下面是某学生一次实验的数据,请完成计算,填入下面的表格中。
坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | 测得晶体中结晶水个数 |
11.7 g | 22.7 g | 17. 6 g | _________ |
(4)这次实验中产生误差的原因可能是__________(填写字母)所造成。
A.硫酸铜晶体中含有易挥发性杂志 B.实验前晶体已部分变白
C.加热时固体部分变黑 D.加热失水后漏置在空气中冷却
(5)已知在坩埚中加热硫酸铜晶体,受热分解过程如下:
CuSO4·5H2O![]() CuSO4·3H2O
CuSO4·3H2O ![]() CuSO4·H2O
CuSO4·H2O ![]() CuSO4
CuSO4
有人借助如图封闭装置进行硫酸铜晶体脱水实验,回答下列问题:
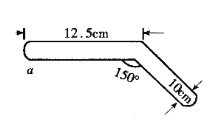
①本实验可用于验证的化学定律是_____________________________。
②a处加热片刻后现象:______________________________________。
③你认为此装置设计是否合理.科学?如不合理,请写出理由:___________________________________________________________________________________________________。