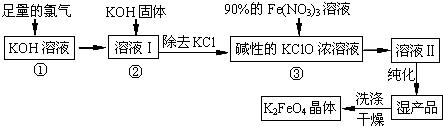
��Ŀ����
2��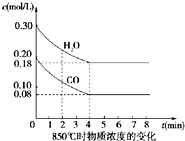 ��һ���Ϊ10L���ܱ������У�ͨ��һ������CO��H2O����850�淢����Ӧ����CO2��H2���ų�������CO��H2OŨ�ȱ仯��ͼ��
��һ���Ϊ10L���ܱ������У�ͨ��һ������CO��H2O����850�淢����Ӧ����CO2��H2���ų�������CO��H2OŨ�ȱ仯��ͼ����1��д���÷�Ӧ�Ļ�ѧ����ʽ��CO+H2O
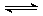 CO2+H2
CO2+H2��2��0-4min��ƽ����Ӧ����v��CO��=0.03mol/��L•min����
��3��850��ʱ��ƽ�ⳣ��K=1��
��4��850��ʱ������������г���1.0mol CO��3.0mol
H2O����CO��ƽ��ת����Ϊ75%��
��5�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������bcf����ѡ����ţ���
a��������ѹǿ���� b�����������c��CO������ c��v����H2��=v����H2O��d��c��CO2��=c��CO��
e�������������ܶȲ��� f��1mol H-H�����ѵ�ͬʱ����2mol H-O����
���� ��1��CO��H2O����850�淢����Ӧ����CO2��H2������Ԫ���غ���д��ѧ����ʽ��
��2������v=$\frac{��c}{��t}$���м��㣻
��3����ͼ��֪��ƽ��ʱc��CO��=0.08mol/Lc����H2O��=0.18mol/L����ƽ��ʱc��CO2��=c��H2��=��c��H2O��=0.3mol/L-0.18mol/L=0.12mol/L������ƽ�ⳣ��K=$\frac{c��CO{\;}_{2}����c��H{\;}_{2}��}{c��CO����c��H{\;}_{2}O��}$���㣻
��4����CO��ת����Ϊx����ת����COΪx mol����
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol����1 3 0 0
�仯����mol����x x x x
ƽ������mol����1-x 3-x x x
��Ӧ��������������䣬�����ʵ�������Ũ�ȴ���ƽ�ⳣ�������x��ֵ���ݴ˼���ת���ʣ�
��5��ƽ���־�����淴Ӧ������ͬ��������ֺ������ֲ��䣬��Ϸ�Ӧ��������ѡ�
��� �⣺��1��CO��H2O����850�淢����Ӧ����CO2��H2����Ӧ�ķ���ʽΪCO+H2O CO2+H2��
CO2+H2��
�ʴ�Ϊ��CO+H2O CO2+H2��
CO2+H2��
��2��v=$\frac{��c}{��t}$=$\frac{��0.20-0.080��mol/L}{4min}$=0.03 mol/��L��min����
�ʴ�Ϊ��0.03��
��3����ͼ��֪��ƽ��ʱc��CO��=0.08mol/Lc����H2O��=0.18mol/L����ƽ��ʱc��CO2��=c��H2��=��c��H2O��=0.3mol/L-0.18mol/L=0.12mol/L����ƽ�ⳣ��K=$\frac{c��CO{\;}_{2}����c��H{\;}_{2}��}{c��CO����c��H{\;}_{2}O��}$=$\frac{0.12��0.12}{0.08��0.18}$=1��
�ʴ�Ϊ��1��
��4����CO��ת����Ϊx����ת���ʵ�COΪx mol����
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol����1 3 0 0
�仯����mol����x x x x
ƽ������mol����1-x 3-x x x
��Ӧ��������������䣬�����ʵ�������Ũ�ȼ���ƽ�ⳣ������K=$\frac{x��x}{��1-x������3-x��}$=1�����x=75%��
�ʴ�Ϊ��75%��
��5��CO��g��+H2 O��g��=CO2��g��+H2��g����H��0����Ӧ�������������ķ��ȷ�Ӧ�����ƽ���ƶ�ԭ������ѡ������淴Ӧ������ͬ��Ӧ�ﵽƽ��״̬��
a����Ӧǰ������������䣬��������ѹǿ�ڷ�Ӧ�����к�ƽ��״̬��ʼ�ղ��䣬���Բ����жϷ�Ӧ�Ƿ���ƽ��״̬����a����
b�����������c��CO�����䣬˵����Ӧ�ﵽƽ��״̬����b��ȷ��
c��v����H2��=v����H2O����˵�����淴Ӧ������ȣ���Ӧ����ƽ��״̬����c��ȷ��
d��c��CO����c��CO2���ı�ֵ����ʼ�����仯���йأ���ֵ���䲻��˵����Ӧ�ﵽƽ��״̬����d����
f��1mol H-H�����ѵ�ͬʱ����2mol H-O����˵�����淴Ӧ������ȣ���ѡbcf��
���� ���⿼���˻�ѧ��Ӧ���ʡ���ѧƽ�ⳣ������ļ���Ӧ�ã�ƽ���־��������������ջ����ǹؼ�����Ŀ�ϼ����⿼�黯ѧƽ����㣬�漰ƽ�ⳣ�����㼰Ӧ�ã��Ѷ��еȣ�ע�⻯ѧƽ�ⳣ������;��1���жϷ�Ӧ���еij̶ȣ�2���жϷ�Ӧ����ЧӦ��3���жϷ�Ӧ���еķ���4������ת���ʵȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | ��״���£�22.4 L H2O�к��еķ�����ΪNA | |
| B�� | 1 mol•L-1 Na2CO3��Һ�к��е���������Ϊ2NA | |
| C�� | 28 g N2�к��е�ԭ����ΪNA | |
| D�� | 1 mol Mg������ϡ���ᷴӦ��ת�Ƶĵ�����Ϊ2NA |
| A�� | �٢ݢڢܢ� | B�� | �٢ۢݢܢ� | C�� | �ۢ٢ݢڢ� | D�� | �ݢڢ٢ۢ� |
 ̼�͵��Ƕ�ֲ�����ڵ���Ҫ���Ԫ�أ�������й����ŷŶ�����̼���������ЧӦ�������������ɹ⻯ѧ������Ŀǰ����Щ�ж��к�����Ĵ�����Ϊ��ѧ�о�����Ҫ���ݣ�
̼�͵��Ƕ�ֲ�����ڵ���Ҫ���Ԫ�أ�������й����ŷŶ�����̼���������ЧӦ�������������ɹ⻯ѧ������Ŀǰ����Щ�ж��к�����Ĵ�����Ϊ��ѧ�о�����Ҫ���ݣ����û���̿��ԭ��������������йط�ӦΪ��C��s��+2NO��g��?N2��g��+CO2��g����ij�о�С����һ���ݻ�������ܱ������������ݻ�Ϊ3L����������������Բ��ƣ��м���NO�������Ļ���̿���ں��£�T�棩�����·�Ӧ����ò�ͬʱ�䣨t��ʱ�����ʵ����ʵ�����n�������
| n/mol t/mol | NO | N2 | CO2 |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | 0.42 | 0.42 |
| 20 | 0.80 | 0.60 | 0.60 |
| 30 | 0.80 | 0.60 | 0.60 |
�ڸ��ݱ������ݣ�����T��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ0.56��������λС������
�����и������жϸ÷�Ӧ�ﵽƽ��״̬����CD
A��������ѹǿ���ֲ��� B.2v��NO����=v��N2����
C��������CO2������������� D�����������ܶȱ��ֲ���
��һ���¶��£�����NO����ʼŨ��������NO��ƽ��ת���ʲ��䣨����������䡱��С������
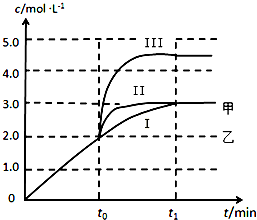
����3L�ݻ��ɱ���ܱ������з�����ӦH2��g��+CO2��g��?H2O��g��+CO��g����������c��CO����ʱ��t�仯������I��ͼ��ʾ������t0ʱ�ֱ�ı�һ������������I�������II������III��
�ٵ�����I�������IIʱ���ı�������Ǽ��������
�ڵ�����I�������IIIʱ���ı���������ı������ı仯���ֱ�������ѹǿ��ѹǿ��Ϊԭ����1.5��
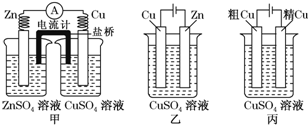
| A�� | ����ԭ��أ����ǵ��װ�� | |
| B�� | �ס���װ���У�п���Ͼ�����������Ӧ | |
| C�� | �ҡ���װ���У�����������������Ӧ���ܽ� | |
| D�� | �ҡ���װ���У�c��Cu2+���������� |