题目内容
10.下列物质中:①空气 ②溶液 ③铜 ④氯气 ⑤二氧化碳 ⑥氧化钙 ⑦氢氧化钠 ⑧硫酸 ⑨碳酸钠 ⑩碳酸钙属于混合物的是①②,属于单质的是③④,属于氧化物的是⑤⑥,属于酸的是⑧,属于盐的是⑨⑩,属于碱的是⑦.
分析 混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物;
单质是有同种元素组成的纯净物;
氧化物是由两种元素组成,一种元素是氧元素;
酸是水溶液中电离出的阳离子全部是氢离子的化合物;
碱是水溶液中电离出的阴离子全部是氢氧根离子的化合物;
盐是金属阳离子和酸根阴离子构成的化合物,铵盐例外.
解答 解:①空气是多种气体的混合物②溶液是分散系,都为混合物;③铜 ④氯气只有一种元素组成是单质;⑤二氧化碳 ⑥氧化钙是由两种元素组成,一种元素是氧元素,是氧化物;⑧硫酸水溶液中电离出的阳离子全部是氢离子,属于酸;⑨碳酸钠 ⑩碳酸钙是金属阳离子和酸根阴离子构成的化合物,属于盐;⑦氢氧化钠属于碱,故答案为:①②;③④;⑤⑥;⑧;⑨⑩;⑦.
点评 本题考查了物质的分类,题目难度不大,注意掌握好物质的分类依据,学习中注意相关基础知识的积累.

练习册系列答案
相关题目
5.下列物质中,不能使紫色石蕊试液变成无色的是( )
| A. | Cl2 | B. | NaClO | C. | Na2O2 | D. | NaOH |
15.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,46gNO2含有2NA个分子 | |
| B. | 标准状况下,1.12L1H2和0.2g2H2均含有0.1NA个质子 | |
| C. | 室温时,1LpH=2的NH4Cl溶液中水电离出H+的数目为10-12NA | |
| D. | 过氧化氢分解制得标准状况下1.12LO2,转移的电子数目为0.2NA |
19.现有如下九种物质:①H2 ②铝 ③CuO ④CO2⑤H2SO4 ⑥Ba(OH)2固体
⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3 ⑩NaHSO4
(1)按物质的分类方法,将上述物质的序号填入表格里的编辑框处:
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH-═H2O,该离子反应对应的化学方程式为Ba(OH)2+2HNO3=Ba(NO3)2+2H2O.
(3)⑨的电离方程式为Al2(SO4)3=2Al3++3SO42-.将34.2g ⑨冷却后溶于水配成250mL溶液,SO42-的物质的量浓度为1.2mol/L.
(4)②与⑧发生反应的化学方程式为:Al+4HNO3(稀)=Al(NO3)3+NO↑+2H2O,该反应的氧化剂是HNO3(填化学式),还原剂与氧化剂的物质的量之比是1:1,当有5.4g Al发生反应时,转移电子的物质的量为0.6mol.
⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3 ⑩NaHSO4
(1)按物质的分类方法,将上述物质的序号填入表格里的编辑框处:
| 分类标准 | 能导电 | 电解质 | 非电解质 |
| 属于该类的物质 | ②⑦⑧⑨ | ③⑤⑥⑨⑩ | ④ |
(3)⑨的电离方程式为Al2(SO4)3=2Al3++3SO42-.将34.2g ⑨冷却后溶于水配成250mL溶液,SO42-的物质的量浓度为1.2mol/L.
(4)②与⑧发生反应的化学方程式为:Al+4HNO3(稀)=Al(NO3)3+NO↑+2H2O,该反应的氧化剂是HNO3(填化学式),还原剂与氧化剂的物质的量之比是1:1,当有5.4g Al发生反应时,转移电子的物质的量为0.6mol.
20.已知:CH4+Br2→CH3Br+HBr
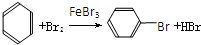
将甲苯和液溴混合在光照下进行反应,得到的产物是( )
①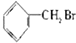 ②
②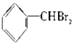 ③
③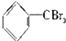 ④
④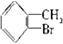 ⑤
⑤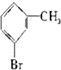
⑥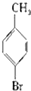 ⑦
⑦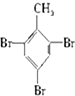
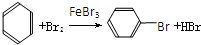
将甲苯和液溴混合在光照下进行反应,得到的产物是( )
①
 ②
② ③
③ ④
④ ⑤
⑤
⑥
 ⑦
⑦
| A. | ①②③ | B. | ⑦ | C. | ④⑤⑥⑦ | D. | 全部 |
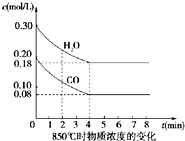 在一体积为10L的密闭容器中,通入一定量的CO和H2O,在850℃发生反应生成CO2和H2并放出热量,CO和H2O浓度变化如图:
在一体积为10L的密闭容器中,通入一定量的CO和H2O,在850℃发生反应生成CO2和H2并放出热量,CO和H2O浓度变化如图: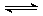 CO2+H2
CO2+H2