题目内容
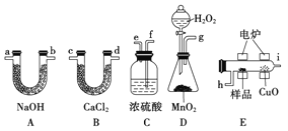
【题目】【化学-选修2:化学与技术】印尼火山喷发不仅带来壮观的美景,还给附近的居民带来物质财富,有许多居民冒着生命危险在底部的火山口收集纯硫磺块来赚取丰厚收入。硫磺可用于生产化工原料硫酸。某工厂用如图所示的工艺流程生产硫酸:

请回答下列问题:
(1)为充分利用反应放出的热量,接触室中应安装 (填设备名称).吸收塔中填充有许多瓷管,其作用是 。
(2)为使硫磺充分燃烧,经流量计1通入燃烧室的氧气过量50%,为提高SO2转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为 .假设接触室中SO2的转化率为95%,b管排出的尾气中二氧化硫的体积分数为 (空气中氧气的体积分数按0.2计),该尾气的处理方法是 。
(3)与以硫铁矿为原料的生产工艺相比,该工艺的特点是 。
A.耗氧量减少
B.二氧化硫的转化率提高
C.产生的废渣减少
D.不需要使用催化剂
(4)硫酸的用途非常广,可应用于下列哪些方面 。
A.橡胶的硫化
B.表面活性剂“烷基苯磺酸钠”的合成
C.铅蓄电池的生产
D.过磷酸钙的制备
(5)矿物燃料的燃烧是产生大气中SO2的主要原因之一.在燃煤中加入适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式 。
【答案】(除标注外,其余每空2分)(1)热交换器(1分) 使浓H2SO4与SO3充分接触
(2)6:5. 0.41% 用氨水吸收(3) AC (1分) (4)BCD
(5)CaCO3![]() CaO+CO2↑、SO2+CaO═CaSO3、2CaSO3+O2═2CaSO4(3分)
CaO+CO2↑、SO2+CaO═CaSO3、2CaSO3+O2═2CaSO4(3分)
【解析】
试题分析:(1)①接触室中进行的反应为SO2的催化氧化,为放热反应,使用热交换器可以充分利用反应放出的热量,对原料气进行预热。吸收塔中填充瓷管的作用是增加接触面积。
(2)S+O2=SO2参加反应的硫黄为1 mol,则经流量计1通入的氧气为1.5 mol,反应后气体总量为1.5 mol×5=7.5 mol,根据反应的方程式2SO2+O2 ![]() 2SO3 可知物质的量之差为0.5 mol,经流量计2通入的氧气为0.5 mol×2.5=1.25 mol,则
2SO3 可知物质的量之差为0.5 mol,经流量计2通入的氧气为0.5 mol×2.5=1.25 mol,则 ![]() =
=![]() =
=![]() 。反应后气体总量为7.5 mol+1.25 mol×5-1 mol×95%×
。反应后气体总量为7.5 mol+1.25 mol×5-1 mol×95%×![]() =13.275 mol,则尾气中SO2的体积分数为
=13.275 mol,则尾气中SO2的体积分数为![]() =0.41%。硫酸工业中,尾气SO2用氨水吸收,再用硫酸处理:SO2+2NH3+H2O=(NH4)2SO3,(NH4)2SO3+H2SO4=(NH4)2SO4+SO2↑+H2O。生成的(NH4)2SO4可作肥料。
=0.41%。硫酸工业中,尾气SO2用氨水吸收,再用硫酸处理:SO2+2NH3+H2O=(NH4)2SO3,(NH4)2SO3+H2SO4=(NH4)2SO4+SO2↑+H2O。生成的(NH4)2SO4可作肥料。
(3)硫铁矿的含硫成分为FeS2,硫元素被氧化生成SO2的同时,铁元素也被氧化生成Fe2O3(废渣),与硫黄直接燃烧相比,耗氧量增加,产生的废渣也增加。答案选AC;
(4)橡胶的硫化是采用硫黄;合成烷基苯磺酸钠需要先合成烷基苯磺酸,而烷基苯磺酸通过烷基苯与浓硫酸的磺化反应生成;铅蓄电池用硫酸作为电解质溶液;过磷酸钙通过磷酸钙与硫酸反应制得。答案选BCD;
(5)CaCO3![]() CaO+CO2↑;SO2+CaO
CaO+CO2↑;SO2+CaO![]() CaSO3;CaSO3不稳定,在空气中容易被氧化成CaSO4。2CaSO3+O2=2CaSO4。
CaSO3;CaSO3不稳定,在空气中容易被氧化成CaSO4。2CaSO3+O2=2CaSO4。

 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案