题目内容
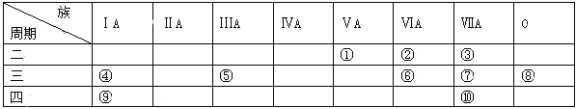
【题目】下表为元素周期表的一部分,请回答有关问题

(1)⑤和⑧的元素符号是_______和_______。
(2)表中最活泼的金属元素是___________,形成化合物种类最多的元素是_________(填写元素名称)。
(3)表中能形成两性氢氧化物的元素是___________,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的化学方程式:__________________;__________________。
(4)证明元素⑥、⑦非金属性强弱,用一个化学方程式表示:_________________________。
【答案】(1)Si、Ar ;
(2)钾,碳;
(3)Al,2Al(OH)3+ 3H2SO4=Al2(SO4)3+ 6H2O,Al(OH)3+ KOH=KAlO2+2H2O;
(4)Cl2+Na2S==2NaCl+S↓.
【解析】试题分析:( 1)⑤ 号元素位于元素周期表中第三周期第ⅣA族是Si元素,⑧号元素是Ar元素,⑤和⑧的元素符号是Si和Ar,答案为:Si、Ar;(2)表中最活跃的金属元素是⑨号元素,⑨号元素是K元素,形成化合物最多的元素是C元素,答案为:钾,碳;(3)在表中的元素中可以形成两性氢氧化物的元素是Al元素,⑥号元素是S元素,最高价氧化物对应水化物是硫酸,氢氧化铝和硫酸反应的化学方程式为2Al(OH)3+ 3H2SO4=Al2(SO4)3+ 6H2O,氢氧化铝和氢氧化钾反应的化学方程式为:Al(OH)3+ KOH=KAlO2+2H2O,答案为:Al,2Al(OH)3+ 3H2SO4=Al2(SO4)3+ 6H2O, Al(OH)3+ KOH=KAlO2+2H2O;(4)硫元素和氯元素非金属性强弱的比较可以通过置换反应比较,将氯气通入硫化钠中如果可以生成S,说明非金属性Cl2>S,答案为:Cl2+Na2S==2NaCl+S↓.

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】氮及其化合物在工业生产和国防建设中有广泛应用。回答下列问题:
(1)氮气性质稳定,可用作保护气。请用电子式表示氮气的形成过程: 。
(2)联氨(N2H4)是一种还原剂。已知:H2O(l)=H2O(g)△H=+44kJ/mol。试结合下表数据,写出N2H4 (g)燃烧热的热化学方程式: 。
化学键 | N—H | N—N | N=N | N≡N | O=O | O—H |
键能(kJ/mol) | 390.8 | 193 | 418 | 946 | 497.3 | 462.8 |
(3)KCN可用于溶解难溶金属卤化物。将AgI溶于KCN溶液中,形成稳定的Ag(CN)2-,该转化的离子方程式为: 。若已知Ksp(AgI)=1.5×10-16,K稳Ag(CN)2-]=1.0×1021,则上述转化方程式的平衡常数K= 。(提示:K稳越大,表示该化合物越稳定)
(4)氨的催化氧化用于工业生产硝酸。该反应可设计成新型电池,试写出碱性环境下,该电池的负极电极反应式: 。
(5)将某浓度的NO2气体充入一恒容绝热容器中,发生反应2NO2![]() N2O4其相关图像如下。
N2O4其相关图像如下。
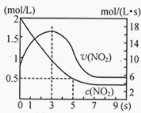
①0~3s时v(NO2)增大的原因是 。
②5s时NO2转化率为 。