题目内容
【题目】在2 L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:

(1)上述反应在第5 s时,NO的转化率为 。
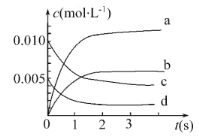
(2)如图中表示NO2变化曲线的是 。用O2表示0~2 s内该反应的平均速率v= 。
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v (O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
【答案】(1)65%; (2)b;0.0015mol·L-1·s-1 ; (3)bc。
【解析】
试题分析:(1)从表中可以看出,开始时n(NO)=0.020mol,5s时n(NO)=0.007mol,转化NO的物质的量为0.013mol,转化率为0.013mol/0.020mol×100%=65%,答案为:65%;(2)根据表中信息可以看出c表示的是NO,d表示O2,转化0.013molNO生成0.013molNO2,所以图上的b才表示NO2,0~2 s内该反应的平均速率用NO表示v(NO)=[(0.020mol-0.008mol)÷2L]/2s=0.003 mol·L-1·s-1,化学反应速率之比等于化学计量系数之比,所以用O2表示0~2 s内该反应的平均速率v=0.0015mol·L-1·s-1,答案为:b;0.0015mol·L-1·s-1;(3)可逆反应达到平衡状态正反应速率等于逆反应速率,各物质的量不变,能说明该反应已达到平衡状态的是: a.v(NO2)=2v (O2),化学反应中任何时候都有化学反应速率之比等于化学计量系数之比,所以a不能说明化学反应达到平衡,a错误; b.容器内压强保持不变,2NO(g)+O2(g)=2NO2(g)是一个气体体积减小的反应,容器内压强不变说明各物质的量不变,化学反应达到平衡,b正确; c.v逆(NO)=2v正(O2),说明正反应速率等于逆反应速率,化学反应达到平衡,c正确; d.容器内密度保持不变,由于气体体积始终不变,气体的质量不变,所以容器内密度始终不变,d错误,答案为:bc。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案





