题目内容
【题目】化学与人类生活密切相关。请按要求,回答下列问题:
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3 + 3Cl2 +10KOH![]() 2 K2FeO4 + 6KCl +8H2O在该反应中,还原剂是____________,当反应中有1mol K2FeO4生成时,消耗的Cl2在标况下的体积为____________L,转移电子的数目为____________。
2 K2FeO4 + 6KCl +8H2O在该反应中,还原剂是____________,当反应中有1mol K2FeO4生成时,消耗的Cl2在标况下的体积为____________L,转移电子的数目为____________。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:_____________________________________________。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_____。
(4)工业上制漂白粉的化学方程式为________________________________,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是_________________________。
(5)KAl(SO4)2·12H2O因其溶于水生成_____(化学式)可以吸附杂质,从而达到净水作用。
(6)硅酸钠水溶液的俗名为__________,可作为木材_______________的原料。
【答案】Fe(OH)3 33.6 3NA或1.806×1024 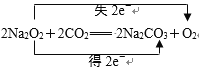 NaHCO3 = Na++HCO3- 2Cl2+2Ca(OH)2= CaCl2+Ca(ClO)2+2H2O 2HClO
NaHCO3 = Na++HCO3- 2Cl2+2Ca(OH)2= CaCl2+Ca(ClO)2+2H2O 2HClO![]() 2HCl +O2↑ Al(OH)3 水玻璃 防火剂
2HCl +O2↑ Al(OH)3 水玻璃 防火剂
【解析】
(1)首先可以判断出高铁酸钾中的铁是+6价,根据方程式可以看出该反应中铁的化合价升高,因此![]() 为还原剂;该反应中每生成2mol高铁酸钾就要消耗3mol氯气,并转移6mol电子,因此当生成1mol高铁酸钾时消耗1.5mol氯气,转移3mol电子,这些氯气在标况下的体积为
为还原剂;该反应中每生成2mol高铁酸钾就要消耗3mol氯气,并转移6mol电子,因此当生成1mol高铁酸钾时消耗1.5mol氯气,转移3mol电子,这些氯气在标况下的体积为![]() L;
L;
(2)该反应是氧元素的歧化反应,一部分氧的化合价升高到0价变为氧气,另一部分氧的化合价降低到-2价变为碳酸钠中的氧,据此来标双线桥即可;
(3)小苏打是盐,盐在水中完全电离用“=”来表示,碳酸是一种弱酸,弱酸酸式盐中的氢是不能完全电离的,因此要写成![]() 的形式;
的形式;
(4)工业制漂白粉的方法是将氯气通入石灰乳中,注意这里只有氯气的化合价发生改变,生成等物质的量的![]() 和
和![]() ;新制氯水在光照下,其中的次氯酸会分解变成氯化氢和氧气,注意不要漏写反应条件;
;新制氯水在光照下,其中的次氯酸会分解变成氯化氢和氧气,注意不要漏写反应条件;
(5)明矾净水的原理是其溶于水后产生的![]() 可以水解变成
可以水解变成![]() 胶体,胶体具有吸附性,因此可以净水;
胶体,胶体具有吸附性,因此可以净水;
(6)硅酸钠的水溶液又名水玻璃,注意这里只能是水溶液,硅酸钠的固体是不能称为水玻璃的,可以用来作木材防火剂的原料。

 名校课堂系列答案
名校课堂系列答案