题目内容
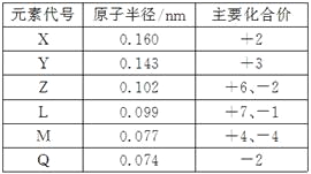
【题目】几种短周期元素的原子半径和主要化合价见下表,下列说法中正确的是( )
A. 等物质的量的X、Y的单质与足量的盐酸反应,生成的H2一样多
B. Y与Q形成的化合物不能跟氢氧化钠溶液反应
C. Z的氢化物的稳定性强于L的氢化物的稳定性
D. 在化学反应中,M原子与其他原子易形成共价键而不易形成离子键
【答案】D
【解析】短周期元素,由元素的化合价可知,Q只有-2价,则为O元素,Z有+6、-2价,可知Z为S元素;L有+7、-1价,则L为氯元素;M有+4、-4价,原子半径L>M,则M为C元素;X为+2价,Y为+3价,原子半径X>Y>Z,所以X为Mg元素,Y为Al元素。结合元素周期律及物质的量结构与性质解答。
短周期元素,由元素的化合价可知,Q只有-2价,则为O元素,Z有+6、-2价,可知Z为S元素;L有+7、-1价,则L为氯元素;M有+4、-4价,原子半径L>M,则M为C元素;X为+2价,Y为+3价,原子半径X>Y>Z,所以X为Mg元素,Y为Al元素。A、X为Mg元素,Y为Al元素,等物质的量的X、Y的单质与足量盐酸反应,根据电子转移守恒可知,二者生成H2为2:3,选项A错误;B、Y与Q形成的化合物为Al2O3,氧化铝是两性氧化物,与氢氧化钠溶液反应生成偏铝酸钠,选项B错误;C、非金属性Cl>S,所以稳定性HCl>H2S,即L的氢化物的稳定性强于Z的氢化物的稳定性,选项C错误;D、M为C元素,最外层电子数为4,电子不易得失,与其它原子易形成共价键而不易形成离子键,选项D正确。答案选D。

练习册系列答案
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目