题目内容
2.在探究SO2性质的实验中,下列说法正确的是( )| A. | SO2气体通入NaOH溶液中,产生倒吸现象,说明SO2极易溶于水 | |
| B. | SO2气体通入溴水中,溴水的颜色褪去,说明SO2具有漂白性 | |
| C. | SO2气体通入酸性KMnO4溶液中,溶液的颜色变浅,说明SO2具有还原性 | |
| D. | SO2气体通入Ba(NO3)2溶液中,溶液出现浑浊现象,说明有BaSO3沉淀生成 |
分析 A.二氧化硫属于酸性氧化物,极易和NaOH反应;
B.二氧化硫具有还原性,溴具有强氧化性,二者发生氧化还原反应;
C.酸性高锰酸钾溶液具有强氧化性,能将二氧化硫氧化;
D.二氧化硫和硝酸钡溶液发生氧化还原反应生成硫酸根离子,硫酸根离子和钡离子发生复分解反应.
解答 解:A.二氧化硫属于酸性氧化物,极易和NaOH反应生成亚硫酸钠,但二氧化硫不是极易溶于水的气体,故A错误;
B.二氧化硫具有还原性,溴具有强氧化性,二者发生氧化还原反应生成硫酸和HBr,二氧化硫体现还原性,故B错误;
C.酸性高锰酸钾溶液具有强氧化性,能将二氧化硫氧化生成硫酸,高锰酸根离子被还原生成锰离子,所以酸性高锰酸钾溶液褪色,二氧化硫体现还原性,故C正确;
D.二氧化硫和硝酸钡溶液发生氧化还原反应生成硫酸根离子,硫酸根离子和钡离子发生复分解反应,所以最后得到的沉淀是BaSO4,故D错误;
故选C.
点评 本题考查二氧化硫性质,二氧化硫具有氧化性、还原性和漂白性,能被强氧化剂氧化而体现还原性,易错选项是D.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
17.X、Y、Z、M、W为五种短周期元素.X原子的质子数与电子层数相同,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示.下列说法不正确的是( )
| Y | Z | M | |
| W |
| A. | 原子半径:W>Y>Z>M>X | |
| B. | 热稳定性:XM>X2Z,沸点:X2Z>YX3 | |
| C. | X、Y、Z三种元素形成的化合物中不可能含离子键 | |
| D. | ZM2、YM3、WM4分子中每个原子最外层均满足8电子结构 |
7.四种短周期元素在周期表中的位置如图,其中只有M为金属元素.下列说法不正确的是( )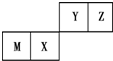

| A. | 原子半径Z<M | |
| B. | Y的最高价氧化物对应水化物的酸性比X的弱 | |
| C. | X的最简单气态氢化物的热稳定性比Z的小 | |
| D. | Z位于元素周期表中第2周期第ⅥA族 |
14.在检验用FeCl3溶液生产铜制印刷线路板后所得的废液成分的实验中,下列根据实验现象得出的结论不正确的是( )
| A. | 向废液中加入少量的葡萄糖溶液,无红色沉淀产生,说明废液中不含Cu2+ | |
| B. | 向废液中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明废液中含有Cl- | |
| C. | 向废液中加少量铁粉,充分反应后无固体剩余,说明废液中含有Fe3+ | |
| D. | 向废液中滴加KSCN溶液,无现象,再加入氯水后溶呈血红色,说明废液中含有Fe2+ |
12.下列说法正确的是( )
| A. | 按系统命名法,化合物(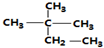 )的名称为2-甲基-2-乙基丙烷 )的名称为2-甲基-2-乙基丙烷 | |
| B. | 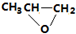 和CO2转化为 和CO2转化为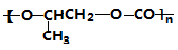 的反应符合绿色化学的原则 的反应符合绿色化学的原则 | |
| C. | 用新制氢氧化铜悬浊液无法检验失去标签的乙醇、乙醛、乙酸三瓶无色溶液 | |
| D. | 乙醇和乙醚互为同分异构体,沸点乙醇比乙醚高 |
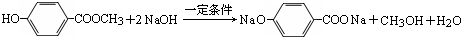 .
.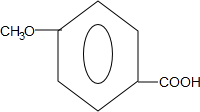 .
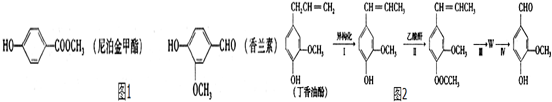
. 和ClCH2CH═CH2 合成丁香油酚的反应类型为取代反应.
和ClCH2CH═CH2 合成丁香油酚的反应类型为取代反应.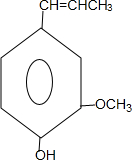 +CH3OCOCOCH3→
+CH3OCOCOCH3→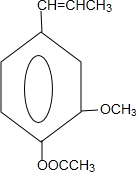 +CH3COOH.
+CH3COOH.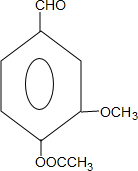 _.
_.
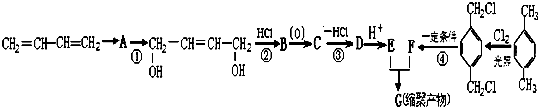
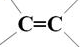 、-COOH.
、-COOH.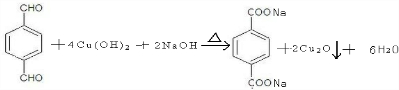 ;
;  .
.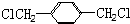 的同分异构体中含有苯环,且苯环上有三个取代基的同分异构体有16种.
的同分异构体中含有苯环,且苯环上有三个取代基的同分异构体有16种.