题目内容
【题目】雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
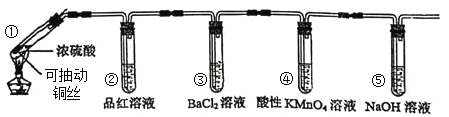
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为____。
(2)上述反应中的氧化剂是____,反应产生的气体可用_____吸收。
(3)As2S3和HNO3有如下反应:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O,若生成2mol H3AsO4,则反应中转移电子的数目为____。
(4)若反应产物NO2与11.2LO2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量___(填字母)。
A.小于0.5mol B.等于0.5mol C.大于0.5mol D.无法确
【答案】1﹕1 As2S3 氢氧化钠溶液或硫酸铜溶液 10NA A
【解析】
(1)根据反应物和生成物来分析反应,若As2S3和SnCl2正好完全反应,As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体,依据电子守恒和原子守恒配平书写化学方程式,利用氧化还原反应反应中得失电子守恒来分析完全反应的物质的量之比来;
(2)根据反应物中某元素化合价的降低来分析氧化剂,并利用气体的性质来分析气体的吸收试剂,硫化氢溶于水为酸,可以和碱溶液反应生成盐和水,也可以利用硫化铜难溶于水和酸,用硫酸铜溶液吸收;
(3)根据氧化还原反应中生成的H3AsO4的物质的量与转移电子数的关系来计算电子转移;
(4)根据NO2与11.2L O2混合后用水吸收全部转化成浓HNO3,4NO2+O2+2H2O═4HNO3,再利用碳与浓硝酸的反应方程式为:C+4HNO3![]() CO2↑+4NO2↑+2H2O,的定量关系来分析计算解答。
CO2↑+4NO2↑+2H2O,的定量关系来分析计算解答。
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体,则反应为2As2S3+2SnCl2+4HCl=As4S4+2SnCl4+2H2S,根据电子得失守恒知1molAs2S3作氧化剂得到2mol电子,而1molSnCl2作还原剂失去2mol电子,则二者的物质的量之比是1:1;
(2)因As2S3在该反应中As元素的化合价降低,则As2S3为氧化剂,又H2S是还原性气体可用碱液吸收或硫酸铜溶液吸收,H2S+2NaOH=Na2S+2H2O,H2S+CuSO4=CuS↓+H2SO4;
(3)由反应As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O可知,As2S3作还原剂,转移电子数为2×(5-3)+3×(0+2)=10,则生成2molH3AsO4时反应中转移电子的物质的量为10mol,电子数为10NA;
(4)由NO2与11.2LO2混合后用水吸收全部转化成浓HNO3,则4NO2+O2+2H2O═4HNO3,氧气的物质的量为![]() =0.5mol,则由反应可知硝酸的物质的量为0.5mol×4=2mol,若硝酸完全反应,C+4HNO3
=0.5mol,则由反应可知硝酸的物质的量为0.5mol×4=2mol,若硝酸完全反应,C+4HNO3![]() CO2↑+4NO2↑+2H2O,则根据化学方程式定量关系可知生成CO2的量是2mol×
CO2↑+4NO2↑+2H2O,则根据化学方程式定量关系可知生成CO2的量是2mol×![]() =0.5mol,但考虑到随着反应到进行,硝酸的浓度会降低而稀硝酸不与碳反应,则产生的CO2的量小于0.5mol,故答案为A。
=0.5mol,但考虑到随着反应到进行,硝酸的浓度会降低而稀硝酸不与碳反应,则产生的CO2的量小于0.5mol,故答案为A。

【题目】元素周期表中第三周期包括Na、Mg、Al、Si、P、S、Cl、Ar 8种元素。请回答下列问题:
(1)SCl2分子中的中心原子杂化轨道类型是_______,该分子构型为_________。
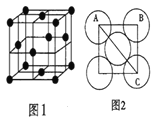
(2)第三周期8种元素按单质熔点(℃)大小顺序绘制的柱形图(已知柱形“1”代表Ar)如图所示,则其中“2”原子的结构示意图为____________,“8”原子的电子排布式为________________。
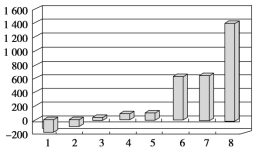
(3)氢化镁储氢材料的晶胞结构如图所示,已知该晶体的密度为ρ g·cm-3,则该晶体的化学式为__________,晶胞的体积为__________cm3(用ρ、NA表示,其中NA表示阿伏加德罗常数的值)。
(4)实验证明:KCl、MgO、CaO三种晶体的结构与NaCl晶体的结构相似,已知NaCl、KCl、CaO晶体的晶格能数据如下表:
晶体 | NaCl | KCl | CaO |
晶格能/(kJ·mol-1) | 786 | 715 | 3401 |
则KCl、MgO、CaO三种晶体的熔点从高到低的顺序是________________。其中MgO晶体中一个Mg2+周围和它最近且等距离的Mg2+有________个。
(5)噻吩(![]() )广泛应用于合成医药、农药、染料工业。
)广泛应用于合成医药、农药、染料工业。
①噻吩分子中含有_______个σ键,分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为![]() ),则噻吩分子中的大π键应表示为______________。
),则噻吩分子中的大π键应表示为______________。
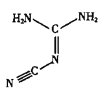
②噻吩的沸点为84℃,吡咯(![]() )的沸点在129~131℃之间,后者沸点较高,其原因是__________________________________。
)的沸点在129~131℃之间,后者沸点较高,其原因是__________________________________。
(6)Si、C和O的成键情况如下:
化学键 | C—O | C===O | Si—O | Si===O |
360 | 803 | 464 | 640 |
C和O之间易形成含有双键的CO2分子晶体,而Si和O之间则易形成含有单键的SiO2原子晶体,请结合数据分析其原因:_______________________________________________________