题目内容
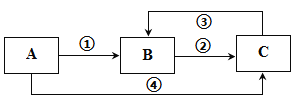
【题目】某同学用下列装置完成了浓硫酸和![]() 性质实验(夹持装置已省略)
性质实验(夹持装置已省略)
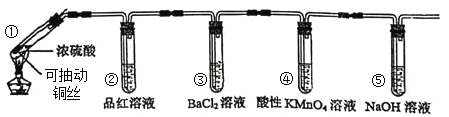
下列说法错误的是
A.反应后,试管①中出现白色固体,将其放入水中溶液显蓝色
B.试管②中品红溶液逐渐褪色,对其加热溶液又恢复红色
C.试管④中酸性高锰酸钾溶液褪色,体现了![]() 的漂白性
的漂白性
D.试管⑤可以改为装有碱石灰的干燥管
【答案】C
【解析】
浓硫酸和铜在加热条件下反应生成SO2,试管②中品红褪色,证明二氧化硫具有漂白性;SO2与氯化钡溶液不反应,则试管③中无现象;酸性高锰酸钾具有强氧化性,能够氧化二氧化硫,则试管④中高锰酸钾褪色;试管⑤为NaOH溶液,用于吸收二氧化硫,防止污染环境,以此解答该题。
A.反应后试管①中的白色固体为硫酸铜,将硫酸铜放入水中,溶液呈蓝色,故A正确;
B.二氧化硫能够漂白品红溶液,二氧化硫的漂白不稳定,加热后又恢复红色,故B正确;
C.试管④中KMnO4溶液褪色,二者发生氧化还原反应,证明SO2具有还原性,故C错误;
D.试管⑤用于吸收二氧化硫,防止污染环境,可以改为装有碱石灰的干燥管,故D正确;
故答案选C。

 天天练口算系列答案
天天练口算系列答案【题目】氯气是一种重要的工业原料,液氯储存区贴有的说明卡如下:
包装 | 钢瓶 |
储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
泄漏处理 | NaOH、NaHSO3溶液吸收 |
下列解释事实的方程式不正确的是
A. 氯气用于自来水消毒:Cl2 + H2O![]() 2H+ + Cl-+ ClO-
2H+ + Cl-+ ClO-
B. 电解饱和食盐水制取Cl2:2Cl- +2H2O![]() 2OH-+ H2↑+Cl2↑
2OH-+ H2↑+Cl2↑
C. 浓氨水检验泄露的氯气,产生白烟:8NH3 + 3Cl2 === 6 NH4Cl + N2
D. 氯气“泄漏处理”中NaHSO3溶液的作用:HSO3-+ Cl2 + H2O === SO42-+ 3H+ + 2Cl-
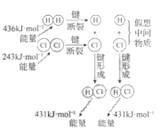
【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
A | B | C | D |
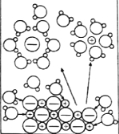
NaCl溶于水 |
电解CuCl2溶液 |
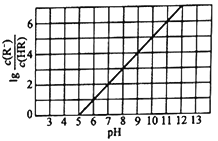
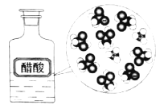
CH3COOH在水中电离 |
H2与Cl2反应能量变化 |
NaCl | CuCl2 | CH3COOH | H2(g)+Cl2(g) ΔH=183kJ·mol1 |
A. AB. BC. CD. D