题目内容
2.下列有关离子方程式与所述事实相符且正确的是( )| A. | Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 用氯化铁溶液和沸水反应制取氢氧化铁胶体:Fe3++3H2O(沸水)═Fe(OH)3↓+3H+ | |
| D. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- |
分析 A.反应生成硫酸钠、硫酸钡和水;
B.电子、电荷不守恒;
C.生成胶体,不是沉淀;
D.反应生成碳酸钙和HClO.
解答 解:A.Ba(OH)2溶液中滴加NaHSO4溶液至中性的离子反应为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故A正确;
B.钠与水反应的离子反应为2Na+2H2O=2Na++2OH-+H2↑,故B错误;
C.用氯化铁溶液和沸水反应制取氢氧化铁胶体的离子反应为Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+,故C错误;
D.漂白粉溶液在空气中失效的离子反应为Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO,故D错误;
故选A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.氮化硅(Si3O4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2+6C+2N2?Si3N4+6CO.下列叙述不正确的是( )
| A. | 若已知上述反应为放热反应,升高温度,其平衡常数减小 | |
| B. | 上述反应中每生成1molSi3N4,转移12mol电子 | |
| C. | 在氮化硅的合成反应中,N2是氧化剂,SiO2是还原剂 | |
| D. | 若使压强增大,上述平衡向逆反应方向移动 |
13.汽车尾气中二氧化硫、氮氧化物和可吸入颗粒物是雾霾主要组成.某课题组用汽车尾气为原料探究二氧化硫、氮氧化物的化学性质.
I.汽车尾气(含有烃类、CO、SO2与NO等物质),冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂).它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化.写出一氧化碳与一氧化氮反应的化学方程式:2CO+2NO?2CO2+N2
Ⅱ.课题组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如图实验装置.请回答:
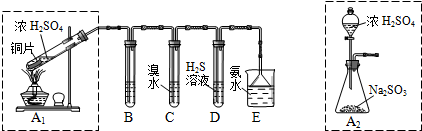
(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为品红溶液;
C中反应的离子方程式为SO2+Br2+2H2O═SO42-+2Br-+4H+.
(2)为了实现绿色环保的目标,制取SO2装置最好选择A2.(A1或A2装置)用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子.请回答:
(3)氨水吸收过量SO2的反应的离子方程式为NH3•H2O+SO2=NH4++HSO3-.
(4))已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/LHNO3、1mol/LBaCl2溶液、l mol/LBa(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO32-、HSO3-,完成下表的实验操作、预期现象和结论:
I.汽车尾气(含有烃类、CO、SO2与NO等物质),冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂).它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化.写出一氧化碳与一氧化氮反应的化学方程式:2CO+2NO?2CO2+N2
Ⅱ.课题组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如图实验装置.请回答:

(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为品红溶液;
C中反应的离子方程式为SO2+Br2+2H2O═SO42-+2Br-+4H+.
(2)为了实现绿色环保的目标,制取SO2装置最好选择A2.(A1或A2装置)用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子.请回答:
(3)氨水吸收过量SO2的反应的离子方程式为NH3•H2O+SO2=NH4++HSO3-.
(4))已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/LHNO3、1mol/LBaCl2溶液、l mol/LBa(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO32-、HSO3-,完成下表的实验操作、预期现象和结论:
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取l mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊,则溶液中存在SO32-或 SO42-. |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体滴入1滴品红,再滴入过量2 mol/L盐酸,振荡 用试管取适量滤液,向其中滴入过量l mol/LBa(OH)2溶液(或1滴品红,再滴入2-3滴2 mol/L盐酸),振荡. 步骤3: | 若品红褪色(或有气泡)则存在SO32- 若出现白色沉淀(或品红褪色或有气泡),则存在HSO3- |
10.根据原子结构及元素周期律的知识,下列推断正确的是( )
| A. | 同主族元素含氧酸的酸性随核电荷数的增加而减弱 | |
| B. | 核外电子排布相同的微粒化学性质也相同 | |
| C. | ${\;}_{17}^{35}$Cl与${\;}_{17}^{37}$Cl得电子能力相同 | |
| D. | F-、O2-、Mg2+、Na+半径逐渐减小 |
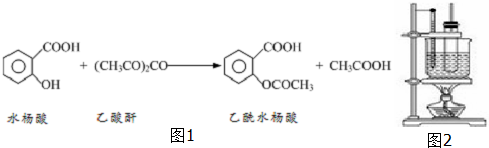
17.工业上常用水杨酸与乙酸酐反应制取解热镇痛药阿司匹林(乙酰水杨酸).
【反应原理】
如图1
【物质性质】
【实验流程】
(1)物质制备:向大试管中依次加入2g水杨酸、5mL乙酸酐(密度为1.08g/mL)、5滴浓硫酸,振荡大试管至水杨酸全部溶解,将其放入盛有热水烧杯中,固定在铁架台上,在85℃~90℃条件下加热5~10min.装置如图2:
(2)产品结晶:取下大试管,置于冷水中冷却10min.待晶体完全析出,…抽滤,再洗涤晶体,抽干.
(3)产品提纯:将粗产品转移至150mL烧杯中,向其中慢慢加入试剂NaHCO3并不断搅拌至不再产生气泡为止.进一步提纯最终获得乙酰水杨酸1.8g.
(4)纯度检验:取少许产品加入盛有5mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色.
【问题讨论】
(1)写出水杨酸与碳酸氢钠溶液反应的化学反应方程式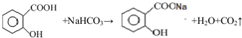 .
.
(2)写出水杨酸与足量碳酸钠溶液反应后含苯环的生成物的结构简式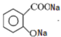 .
.
(3)流程(1)装置图中长导管的作用冷凝回流和平衡压强.
(4)控制反应温度85℃~90℃的原因既保持有较高的反应速率又减少物质的挥发.
(5)流程(2)中证明晶体洗涤干净的操作方法:取最后一次洗涤滤液少许于试管中,滴加少量氯化钡,再滴加稀盐酸,若无沉淀出现则洗涤干净,反之则未洗涤干净
(6)流程(4)中溶液显紫色,可能的原因是产品中仍然可能有水杨酸.
(7)1mol乙酰水杨酸与氢氧化钠溶液反应可能,最多消耗3mol NaOH.
(8)实验中乙酰水杨酸的产率为69%(已知:水杨酸、乙酰水杨酸的相对分子质量分别为138和180).
【反应原理】
如图1

【物质性质】
| 试剂 | 沸点(℃) | 溶解度 | 化学性质 |
| 乙酸酐 | 139 | 在水中逐渐分解 | 略 |
| 乙酰水杨酸 | 略 | 微溶于水 | 与碳酸钠反应生成水溶性盐 |
| 水杨酸 | 211 | 微溶于冷水,易溶于热水 | 略 |
| 乙酸 | 117.9 | 略 | 略 |
(1)物质制备:向大试管中依次加入2g水杨酸、5mL乙酸酐(密度为1.08g/mL)、5滴浓硫酸,振荡大试管至水杨酸全部溶解,将其放入盛有热水烧杯中,固定在铁架台上,在85℃~90℃条件下加热5~10min.装置如图2:
(2)产品结晶:取下大试管,置于冷水中冷却10min.待晶体完全析出,…抽滤,再洗涤晶体,抽干.
(3)产品提纯:将粗产品转移至150mL烧杯中,向其中慢慢加入试剂NaHCO3并不断搅拌至不再产生气泡为止.进一步提纯最终获得乙酰水杨酸1.8g.
(4)纯度检验:取少许产品加入盛有5mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色.
【问题讨论】
(1)写出水杨酸与碳酸氢钠溶液反应的化学反应方程式
 .
.(2)写出水杨酸与足量碳酸钠溶液反应后含苯环的生成物的结构简式
 .
.(3)流程(1)装置图中长导管的作用冷凝回流和平衡压强.
(4)控制反应温度85℃~90℃的原因既保持有较高的反应速率又减少物质的挥发.
(5)流程(2)中证明晶体洗涤干净的操作方法:取最后一次洗涤滤液少许于试管中,滴加少量氯化钡,再滴加稀盐酸,若无沉淀出现则洗涤干净,反之则未洗涤干净
(6)流程(4)中溶液显紫色,可能的原因是产品中仍然可能有水杨酸.
(7)1mol乙酰水杨酸与氢氧化钠溶液反应可能,最多消耗3mol NaOH.
(8)实验中乙酰水杨酸的产率为69%(已知:水杨酸、乙酰水杨酸的相对分子质量分别为138和180).
7.下列各组中,互为同位素的是( )
| A. | O2和O3 | B. | 3517R和3717R | C. | 2311X和2311X+ | D. | 4018R和4020X |
14.下列哪种物质所含原子数与0.2molH3PO4所含原子数相等( )
| A. | 0.4molH2O | B. | 0.2mol H2SO4 | C. | 0.8molHCl | D. | 0.3molHNO3 |
10.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1L lmol•L-1 FeBr2溶液与lmol氯气反应时转移的电子数为3NA | |
| B. | 0.5 mol•L-1硫酸钠溶液中含有溶质离子总数为1.5NA | |
| C. | 1mol硫酸氢钠固体中含阳离子总数NA | |
| D. | 28g由乙烯和聚乙烯组成的混合气体中含有碳碳双键数为NA |
10.下列电离方程式中,错误的是( )
| A. | H2CO3?H++HCO3-; HCO3-?H++CO32- | B. | H2SO4═2H++SO42- | ||
| C. | NaHS═Na++H++S2- | D. | CH3COOH?H++CH3COO- |