题目内容
12.某一化学反应中,其产物的总能量为80kJ,如果该反应是放热反应,那么反应物的总能量可能是( )| A. | 100KJ | B. | 60KJ | C. | 50KJ | D. | 30KJ |
分析 根据放热反应中,反应物的总能量高于生成物的总能量.
解答 解:因放热反应中,反应物的总能量高于生成物的总能量,产物的总能量为80kJ,所以反应物总能量大于80kJ,
故选A.
点评 本题主要考查了放热反应中反应物的总能量与生成物的总能量的关系,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.下列说法中正确的是( )
| A. | 淀粉和蛋白质水解的最终产物都只有一种 | |
| B. | 蔗糖和淀粉都不能发生氧化反应 | |
| C. | 棉花、合成纤维、ABS树脂、蚕丝和核酸都属于高分子化合物 | |
| D. | 石油裂解和油脂皂化都是由高分子生成小分子的过程 |
20.下列各分子中,构成分子的原子不处在同一平面上的是( )
| A. | 甲烷 | B. | 乙烯 | C. | 乙炔 | D. | 苯 |
7.下列说法正确的是( )
| A. | 离子键就是使阴、阳离子结合成化合物的静电引力 | |
| B. | 含有离子键的化合物一定是离子化合物 | |
| C. | 所有金属与所有非金属之间都能形成离子键 | |
| D. | 在化合物Na2O2中,阴、阳离子的个数比为1:1 |
4.下列描述正确的是( )
| A. | 氯气、SO2都能使品红溶液褪色,它们的漂白原理相同 | |
| B. | 滴加石蕊试液显红色的溶液:Fe3+、NH4+、I-可能大量共存 | |
| C. | 某溶液中加入盐酸酸化的氯化钡产生白色沉淀,原溶液中一定含有SO42- | |
| D. | Fe(NO3)2溶液中滴加少量稀硫酸会变黄色 |
1.为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$,则下列叙述正确的是( )
| A. | 中性溶液的 AG=0 | B. | 酸性溶液的AG<0 | ||
| C. | 常温下0.1mol/LNaOH溶液的AG=12 | D. | 常温下0.1mol/L盐酸溶液的AG=12 |
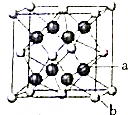 A、B、C、D、E原子序数依次增大,且为前四周期的元素,其中B2-和C+具有相同的核外电子排布;D的氢化物的沸点比其上一周期同族元素氢化物的沸点低;E核外有五个单电子,B、E形成的某种化合物和A、D形成的化合物的浓溶液加热时反应可用于实验时制取气态单质D.
A、B、C、D、E原子序数依次增大,且为前四周期的元素,其中B2-和C+具有相同的核外电子排布;D的氢化物的沸点比其上一周期同族元素氢化物的沸点低;E核外有五个单电子,B、E形成的某种化合物和A、D形成的化合物的浓溶液加热时反应可用于实验时制取气态单质D. 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1.请回答下列问题:
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1.请回答下列问题: