题目内容
【题目】化学研究小组探究外界条件对化学反应mA(g)+nB(g)![]() pC(g)+qD(g)的速率和平衡的影响图像如下,下列判断错误的是( )
pC(g)+qD(g)的速率和平衡的影响图像如下,下列判断错误的是( )
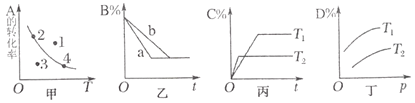
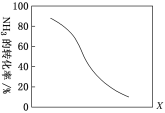
A.甲图中,表示反应速率v正>v逆的是点1
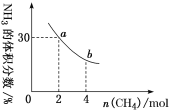
B.乙图中,若m+n=p+q,则a曲线可能使用了催化剂
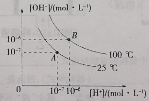
C.由丙图可知,T1<T2,该反应正反应为放热反应
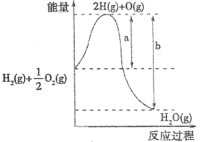
D.由丁图可知,该反应m+n>p+q
【答案】A
【解析】
A.甲图中曲线上各点均处于平衡状态,点1的转化率大于平衡转化率,点1应逆向进行建立平衡,则点1的反应速率:v正<v逆,故A错误;
B.乙图中,若m+n=p+q,表示该反应为气体体积不变的反应,图中a、b的平衡状态相同,则a曲线先达到平衡,可能使用了催化剂或增大了压强,故B正确;
C.丙图中,T2先达到平衡,则T1<T2;T2对应C%含量低,则升高温度,平衡逆向移动,说明正反应为放热反应,故C正确;
D.丁图中,相同温度下,压强越大,C%含量越高,则增大压强,平衡正向移动,则m+n>p+q,故D正确;
故选A。

练习册系列答案
相关题目