题目内容
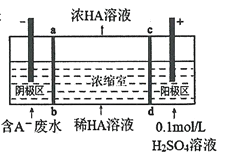
【题目】用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。下列有关叙述不正确的是( )
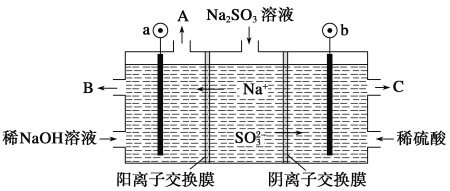
A.图中a极连接电源的负极
B.A口放出的物质是氢气,C口放出的物质是氧气
C.b极电极反应式为:SO32--2e-+H2O===SO42-+2H+
D.电解过程中阴极区碱性明显增强
【答案】B
【解析】
试题分析:A、Na+移向阴极区,SO32-移向阳极区,所以a极为阴极,应接电源负极,故A正确;B、阴极区放电离子为氢离子生成氢气,阴极电极反应式为2H2O+2e-═H2↑+2OH-,A口出来的是氢气,b极应接电源正极,阳极电极反应式为SO32--2e-+H2O═SO42-+2H+,所以A口放出的物质是氢气,从C口流出的是浓度较大的硫酸,故B错误;C、b为阳极,SO32-在阳极失去电子变成SO42-,阳极电极反应式为SO32--2e-+H2O═SO42-+2H+,故C正确;D、在阴极区,由于H+放电,破坏水的电离平衡,c(H+)减小,c(OH-)增大,生成NaOH,碱性增强,故D正确。

 名校课堂系列答案
名校课堂系列答案【题目】过氧化钙(CaO2)常用作种子及谷物的无毒性消毒剂,常温下为白色的固体,微溶于水,且不溶于乙醇、乙醚和碱性溶液,但溶于酸。某实验小组拟探究CaO2的性质及其实验室制法。
(1)实验探究CaO2与酸的反应。
操作 | 现象 |
向盛有4gCaO2的大试管中加入10mL稀盐酸得溶液a | 剧烈反应,产生能使带火星木条复燃的气体 |
取5mL溶液a置于试管中,滴入两滴石蕊溶液 | 溶液变红,一段时间后溶液颜色明显变浅,稍后溶液变为无色 |
①CaO2与盐酸反应的化学方程式为_____________。
②加入石蕊溶液后溶液褪色可能是因为溶液a中存在较多的_____________。
(2)用如图所示装置制备过氧化钙,其反应原理为Ca+O2![]() CaO2。
CaO2。
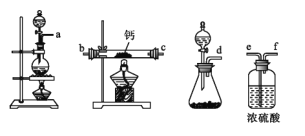
①请选择实验所需要的装置,按气流方向连接的顺序为_____________(填仪器接口的字母,上述装置可不选用也可重复使用)。
②根据完整的实验装置进行实验,实验步骤如下:Ⅰ.检验装置的气密性后,装入药品;Ⅱ.打开分液漏斗活塞,通入气体一段时间,加热药品;Ⅲ.反应结束后,_____________(填操作);Ⅳ.拆除装置,取出产物。
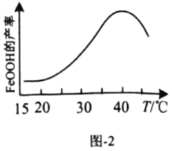
(3)利用反应Ca2++H2O2+2NH3+8H2O=CaO28H2O↓+2![]() 在碱性环境下制取CaO2的装置如图所示。
在碱性环境下制取CaO2的装置如图所示。
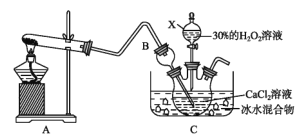
①NH3在Ca2+和H2O2的反应过程中所起的作用是_____________。
②反应结束后,经过滤、洗涤、低温烘干可获得CaO28H2O。过滤需要的玻璃仪器是_____________;将沉淀进行洗涤的操作为_____________。