题目内容
14.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )| A. | 常温常压下,20 g D2O和足量的金属钠反应产生气体的分子数为0.5NA | |
| B. | 1 mol Na2O2与足量的水反应,转移的电子数为2NA | |
| C. | NA 个SO3分子在标准状况下的体积为22.4 L | |
| D. | 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA |
分析 A.根据n=$\frac{m}{M}$计算水的物质的量,根据方程式计算生成的气体,再根据N=nNA计算分子数目.
B.过氧化钠与水反应,过氧化钠既做氧化剂又做还原剂;
C.标况下,三氧化硫不是气体;
D.依据PH计算氢离子浓度,结合溶液中离子积常数计算碱溶液中氢氧根离子浓度.
解答 解:A.20gD2O的物质的量为1mol,钠与水反应2Na+2D2O=2NaOD+D2↑,由方程式可知,1mol水反应生成D20.5mol,D2的分子数为0.5mol×NAmol-1=0.5NA;故A正确;
B.过氧化钠与水反应,过氧化钠既做氧化剂又做还原剂,1 mol Na2O2与足量的水反应,转移的电子数为NA,故B错误;
C.标况下,三氧化硫不是气体,不能使用气体摩尔体积,故C错误;
D.A、pH=13,即C(H+)=10-13mol/L,C(OH-)=$\frac{10{\;}^{-14}}{1{0}^{-13}}$mol/L=0.1mol/L,根据n=CV=0.1mol/L×1.0L=0.1mol,个数为NA个,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的应用,握公式的使用和物质的结构是关键,注意气体摩尔体积的条件应用,题目难度不大.

练习册系列答案
相关题目
4.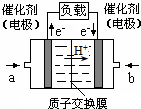 可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法中正确的是( )
可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法中正确的是( )
 可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法中正确的是( )
可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法中正确的是( )| A. | 右边的电极为电池的负极,b处通入的是空气 | |
| B. | 左边的电极为电池的负极,a处通入的是甲醇 | |
| C. | 电池负极的反应式为:CH3OH+H2O═CO2+6H++4e- | |
| D. | 电池正极的反应式为:O2+2H2O+4e-═4OH- |
2.下列微粒中,对水的电离平衡不产生影响的是( )
| A. | 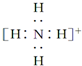 | B. | 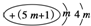 | C. | 26R3+ | D. | 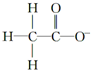 |
9.下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是( )
| A. | 甲烷与氯气发生取代反应 | |
| B. | 丙烯与水在催化剂的作用下发生加成反应 | |
| C. | 异戊二烯[CH2═C(CH3)-CH═CH2]与等物质的量的Br2发生加成反应 | |
| D. | 2-氯丁烷(CH3CH2CHClCH3)与NaOH乙醇溶液共热 |
19.硼酸(H3BO3)分子的中心原子B最外层电子并未达到饱和,它在水中结合水分子电离出来的OH-使B原子最外层电子达到饱和,电离过程如图所示.下列表述正确的是( )
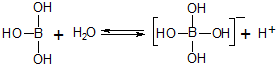
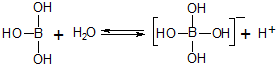
| A. | 硼酸加入水中抑制水的电离 | |
| B. | 硼酸是三元酸 | |
| C. | 硼酸与强碱在溶液中反应:H3BO3+OH-═[B(OH)4]- | |
| D. | 硼酸是两性化合物 |
6.下列说法正确的是( )
| A. | ${\;}_{53}^{131}$I与${\;}_{53}^{125}$I 互为同位素 | |
| B. | ${\;}_{53}^{131}$I与${\;}_{53}^{125}$I性质完全相同 | |
| C. | ${\;}_{94}^{224}$Pu位于周期表中第六周期 | |
| D. | ${\;}_{53}^{131}$I的质子数为78 |
3.如图是氢氧燃料电池构造示意图.关于该电池的说法不正确的是( )


| A. | a极是正极 | B. | 电池总反应式为:2H2+O2=2H2O | ||
| C. | 电子由b通过灯泡流向a | D. | 氢氧燃料电池是环保电池 |

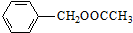 是其中的一种,该有机物能发生的反应为a(填字母).
是其中的一种,该有机物能发生的反应为a(填字母).