题目内容
6.“安全生产,人命关天”.国家对易燃、易爆物的生产、贮存、运输、使用有严格规定,绝不允许违章操作.下列混合物,遇明火可能发生爆炸的是( )| A. | 一氧化碳和氢气的混和气 | |
| B. | 碳在氧气中不完全燃烧得到的混和气 | |
| C. | 电解水正极与负极气体形成的混和气 | |
| D. | 氮气和氧气的混和气 |
分析 根据爆炸的原理或发生的条件判断,爆炸是可燃性物质在有限的空间中燃烧,燃烧放出的热量聚集不能散失,气体受热急剧膨胀造成的,可燃性的气体与氧气或空气混合后点燃易发生爆炸.
解答 解:可燃性气体或物质与空气混合后的遇明火、静电、电火花或加热易爆炸.
A、碳在氧气中不完全燃烧得到的混和气是一氧化碳和二氧化碳的,没有支持燃烧的气体,不能发生爆炸,故A错误;
B、二氧化碳不燃烧,也不支持燃烧,与空气混合后遇明火,不可能发生爆炸,故B错误;
C、电解水正极与负极气体形成的混和气是氢气和氧气,遇明火可能发生爆炸,故C正确;
D、氮气和氧气中没有能够燃烧的气体,遇到明火不可能发生爆炸,故D错误.
故选C.
点评 “生命重于泰山”安全问题无小事,尤其是防火、防爆问题,所以燃烧和爆炸知识就成了化学考查热点,要注意燃烧爆炸的条件和防护措施.本题主要考查了可燃物与空气混合遇明火是否爆炸的内容.

练习册系列答案
相关题目
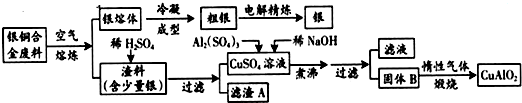
18.某工业生产的废液中含有FeCl2、FeCl3、AlCl3、MnCl2,欲从中提取MnCl2,方案如下:加H2O2溶液氧化;调节pH,产生沉淀X;过滤,得MnCl2溶液.已知各金属离子沉淀的pH范围如下:
(1)加入H2O2的目的是将亚铁离子氧化为铁离子;调节pH的范围是4.7~7.8;
(2)向沉淀X中加入NaOH溶液,有关反应的化学方程式为NaOH+Al(OH)3=NaAlO2+2H2O,过滤后将所得沉淀加热后得红棕色固体,写出高温下该固体与金属铝的反应方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe;
(3)一定条件下电解含Mn2+的溶液可以制得MnO2,生成MnO2的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+,同时在另一极还能获得一种清洁能源是H2.
| 离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ |
| 开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 |
| 沉淀完全的pH | 3.7 | 4.7 | 9.6 | 9.8 |
(2)向沉淀X中加入NaOH溶液,有关反应的化学方程式为NaOH+Al(OH)3=NaAlO2+2H2O,过滤后将所得沉淀加热后得红棕色固体,写出高温下该固体与金属铝的反应方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe;
(3)一定条件下电解含Mn2+的溶液可以制得MnO2,生成MnO2的电极反应式为Mn2+-2e-+2H2O=MnO2+4H+,同时在另一极还能获得一种清洁能源是H2.
14.下列物质的化学式书写正确是( )
| A. | 氯化钠( ClNa ) | B. | 高锰酸钾(K2MnO4) | C. | 硫酸钠(Na2S) | D. | 碳酸(H2CO3) |
1.下面是同学们学习化学后总结的安全常识,其中有错误的是( )
| A. | 煤气泄漏--严禁开关电器 | |
| B. | 进入加油站--严禁拨打手机 | |
| C. | 逃离火灾现场--用湿毛巾堵住口鼻 | |
| D. | 防止白磷自燃--将其放在煤油中密封 |
11.美国加州爱德华空军基地的空军研究室,研究高能材料的化学家宣布合成并表征了一种含有N5+离子的盐类,该阳离子可看作是100多年来第三次可分离获得的全氮物种,下列有关N5+离子的叙述不正确的是( )
| A. | 它是一种阳离子 | B. | 该离子所含质子总数比电子总数多 | ||
| C. | 一个N5+离子中有36个质子 | D. | N5+离子中含有34个电子 |
 溶液再生,其装置示意图如下:
溶液再生,其装置示意图如下: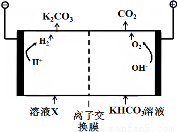
 H2O+CO2↑。
H2O+CO2↑。 O2(g)
O2(g) O2(g)
O2(g)
 生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:
生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下: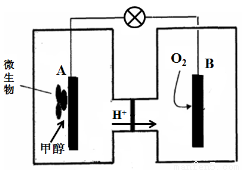 、
、