题目内容
【题目】室温下某溶液中由水电离产生的c(H+)等于10-10mol·L-1,该溶液的溶质不可能是( )
A.NaHSO4B.NaClC.HClD.Ba(OH)2
【答案】B
【解析】
A.硫酸氢钠能电离出氢离子,抑制水的电离,故可能是硫酸氢钠;
B.氯化钠对水的电离无影响,故符合题意;
C.盐酸抑制水的电离,故不符合题意;
D.氢氧化钡电离出氢氧根离子,抑制水的电离,不符合题意。
故选B。

【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,研究甲醇具有重要意义。有人模拟用CO和H2合成甲醇,其反应为:CO(g) + 2H2(g) CH3OH(g) △H<0
(1)在容积固定为1L的密闭容器内充入2 mol CO和4 mol H2发生上述反应,20min时用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
压强/MPa | 12.4 | 10.2 | 8.4 | 7.0 | 6.2 | 6.2 |
则反应从开始到20min时,以CO浓度变化表示的平均反应速率v(CO)=_________mol/(L·min),该温度下平衡常数K=___________,若平衡后增大压强,则K值_________(填“增大”、“减小”或“不变”)。
(2)在恒温恒容的密闭容器中,不能判定CO(g)+2H2(g) CH3OH(g) △H<0,反应达到平衡的是___________;
A、压强保持不变 B、气体的密度保持不变
C、气体平均摩尔质量保持不变 D、速率v(H2):v(CH3OH)=2:1
(3)如图是甲醇燃料电池结构示意图,C是________(填“正”或“负”)极,写出此电极的电极反应式__________________________________________。

(4)若以该电池为电源,用石墨做电极电解100mL CuSO4溶液,电解一段时间后,两极均收集到11.2L的气体(标准状况下),则原CuSO4溶液的物质的量浓度为________mol/L。
【题目】(1)有关研究需要得到反应C3H8(g)===3C(石墨,s)+4H2(g)的ΔH,但测定实验难进行。设计下图可计算得到:

①ΔH______0(填“>”、“<”或“=”)。
②ΔH=____________________(用图中其他反应的反应热表示)。
(2)已知在压强为a MPa、500℃下,2 mol H2和1 mol CO2在某密闭容器中反应,生成水和气态二甲醚CH3OCH3 。其中CO2的转化率为60%,此过程中放出0.3Q kJ热量。此反应的热化学方程式为_____________。
(3)下表是部分化学键的键能数据:
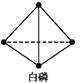
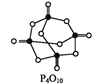
化学键 | P—P | P—O | O=O | P=O |
键能/(kJ·mol-1) | 198 | 360 | 498 | x |
已知,白磷在空气中燃烧生成P4O10,白磷的燃烧热为2 982 kJ·mol-1,白磷(P4)、P4O10结构如图所示,则上表中x=____。