题目内容
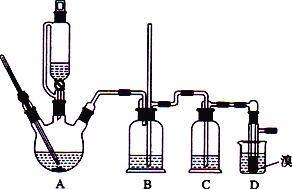
【题目】实验室用CH3CH2OH分两步制备1,2-二溴乙烷现用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
有关数据列表如下:
物质名称 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/(g·cm-3) | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)装置A中发生的化学方程式为_________________________________,反应类型为________,在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是________(填字母)。
a 引发反应 b减少副产物乙醚生成 c 防止乙醇挥发 d加快反应速率
(2)在装置C中应加入________(填字母),其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3) 装置D中实验现象为_______________。
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在________(填“上”或“下”)层。
(5)反应过程中应用冷水冷却装置D,其主要目的是____________________________。
【答案】C2H5OH ![]() CH2=CH2↑+ H2O 消去反应 b c 溴的颜色完全褪去 下 避免溴大量挥发
CH2=CH2↑+ H2O 消去反应 b c 溴的颜色完全褪去 下 避免溴大量挥发
【解析】
装置A为乙烯的制备装置,装置B是根据气压原理设计的防堵塞装置,如果D中导气管发生堵塞,A中产生的乙烯气体会导致装置B中压强增大,长导管液面会上升,浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,装置C中盛有的氢氧化钠溶液吸收酸性气体,防止干扰1,2-二溴乙烷的制备,装置D是溴水与乙烯反应生成1,2-二溴乙烷的反应器。
(1)装置A中乙醇在浓硫酸作用下,170℃时发生消去反应生成乙烯,反应的化学方程式为C2H5OH ![]() CH2=CH2↑+ H2O;乙醇与浓硫酸的混合液共热的温度控制在140℃,乙醇分子间脱去一个水分子,反应生成的是乙醚,所以制备乙烯实验中,要尽可能迅速地把反应温度提高到170 ℃左右,减少副产物乙醚生成,故答案为:C2H5OH
CH2=CH2↑+ H2O;乙醇与浓硫酸的混合液共热的温度控制在140℃,乙醇分子间脱去一个水分子,反应生成的是乙醚,所以制备乙烯实验中,要尽可能迅速地把反应温度提高到170 ℃左右,减少副产物乙醚生成,故答案为:C2H5OH ![]() CH2=CH2↑+ H2O;消去反应;b;
CH2=CH2↑+ H2O;消去反应;b;
(2)浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,二氧化碳、二氧化硫能和氢氧化钠溶液反应,故答案为:c;
(3)乙烯和溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷为无色,所以装置D中实验现象为溴的颜色完全褪去,故答案为:溴的颜色完全褪去;
(4)1,2-二溴乙烷和水不互溶,1,2-二溴乙烷密度比水大,所以加水,振荡后静置,产物应在下层,故答案为:下;
(5)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,故答案为:避免溴大量挥发。

 阅读快车系列答案
阅读快车系列答案【题目】利用化学原理对工厂排放的废水、废渣等进行有效检测与合理处理。
某工厂对制革工业污泥中Cr元素的回收与再利用工艺如图(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+):
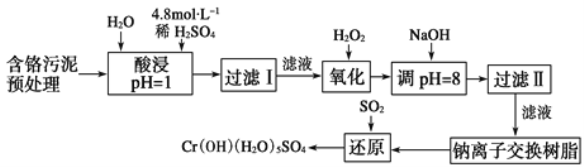
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | - | - | - |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 9(>9溶解) |
(1) 酸浸时,为了提高浸取率可采取的措施是____(至少写两条)。
(2)H2O2的作用是_____。
(3)调pH=8是为了除去___(填Fe3+、Fe2+、Al3+、Ca2+、Mg2+)。
(4)钠离子交换树脂的原理为Mn++nNaR→MRn+nNa+,被交换的杂质离子是___(填Fe3+、Fe2+、Al3+、Ca2+、Mg2+)。
(5)已知以下氧化还原反应方程式(未配平):Na2Cr2O7+SO2+H2O=Cr(OH)(H2O)5SO4+Na2SO4;以上反应各物质的配平系数依次为___。每生成1 mol Cr(OH)(H2O)5SO4转移电子的数目为___。