题目内容
8.关于下图所示转化关系(X代表卤素),说法不正确的是( )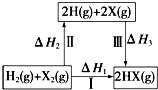
| A. | 2H(g)+2X(g)═2HX(g)△H3<0 | |
| B. | 生成HX的反应热与途径无关,所以△H1=△H2+△H3 | |
| C. | F、Cl、Br的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多 | |
| D. | F2、Cl2分别发生反应I,同一温度下的平衡常数分别为K1、K2,则K1>K2 |
分析 A、原子形成化学键放热,焓变小于0;
B、依据盖斯定律分析,反应焓变与起始物质和终了物质有关于变化途径无关;
C、途径Ⅱ是断裂化学键的过程,是吸热过程,F、Cl、Br的原子半径依次增大,F2、Cl2、Br2断裂化学键需要能量依次减小;
D、根据F2的氧化性大于Cl2,所以F2与氢气化合的程度比Cl2大,据此判断平衡常数大小;
解答 解:A、原子形成化学键放热,焓变小于0,2H(g)+2X(g)═2HX(g)△H3<0,故A正确;
B、反应焓变与起始物质和终了物质有关于变化途径无关,途径Ⅰ生成HX的反应热与途径无关,所以△H1=△H2+△H3 ,故B正确;
C、F、Cl、Br的原子半径依次增大,F2、Cl2、Br2断裂化学键需要能量依次减小,所以途径Ⅱ吸收的热量依次减小,故C错误;
D、因F2的氧化性大于Cl2,所以F2与氢气化合的程度比Cl2大,则F2、Cl2分别发生反应I,同一温度下的平衡常数分别为K1>K2,故D正确;
故选C.
点评 本题考查了合成反应能量变化,反应焓变分析判断,物质结构和同主族性质变化规律是解题关键,题目难度中等.

练习册系列答案
相关题目
19.下列过程没有发生化学反应的是( )
| A. | 往鲜榨苹果汁中加入适量柠檬汁防止苹果汁变色 | |
| B. | 做馒头时加一些面碱(Na2CO3)避免馒头发酸 | |
| C. | 采用添加有“光触媒”的硅藻泥做装饰材料,净化室内空气,避免装修污染 | |
| D. | 用汽油洗掉衣物沾上的油渍 |
16.下列关于同系物及同分异构体的说法,错误的是( )
| A. | 同分异构体因结构不同,化学性质一定差别很大 | |
| B. | 具有相同通式的有机物不一定互为同系物 | |
| C. | 两个相邻同系物的相对分子质量数值一定相差14 | |
| D. | 同分异构体不可能互为同系物 |
3.甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料,其结构如图所示.下列说法中错误的是( )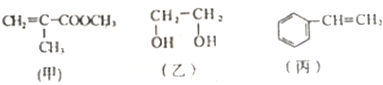
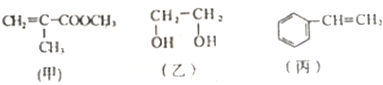
| A. | 甲物质可以在引发剂作用下生成有机高分子化合物 | |
| B. | 甲、乙、丙三种物质都可以发生加成反应 | |
| C. | 丙物质能够使酸性高锰酸钾溶液褪色 | |
| D. | 1mol乙物质可与2mol钠完全反应生成1mol氢气 |
13.关于溴乙烷与NaOH的乙醇溶液反应的现象和产物检验,说法正确的是( )
| A. | 往反应后的溶液中加入AgNO3溶液检验是否有Br-生成 | |
| B. | 实验中观察不到有气体生成 | |
| C. | 生成的气体可直接通入到溴水中检验是否有乙烯生成 | |
| D. | 生成的气体可直接通入到酸性高锰酸钾溶液中检验是否有乙烯生成 |
17.下列说法不正确的是( )
| A. | ${\;}_{55}^{133}Cs$和${\;}_{55}^{137}Cs$互为同位素 | |
| B. | ${\;}_{67}^{166}Ho$的原子核内的中子数与核外电子数之差为32 | |
| C. | 元素周期表中L层电子为奇数的元素所在族序数与该元素原子的L层电子数相等 | |
| D. | 1 mol KHSO4加热熔化可电离出2NA个阳离子 |
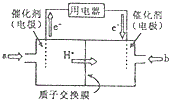 二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或H2SO4反应生成SeO2以回收Se.完成下列填空:
二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或H2SO4反应生成SeO2以回收Se.完成下列填空: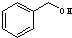 与
与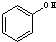 ⑥
⑥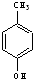 与
与