题目内容
9.有机物分子中原子之间(或原子与原子团之间)的相互影响会导致物质化学性质的不同.下列事实不能说明上述观点的是( )| A. | 乙醇不能与NaOH溶液反应,苯酚则能跟NaOH溶液反应 | |
| B. | 乙醛一定条件下能与氢气发生加成反应,乙酸一般不能与氢气发生加成反应 | |
| C. | 苯不能使酸性高锰酸钾溶液褪色,甲苯则能使酸性高锰酸钾溶液褪色 | |
| D. | 苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应 |
分析 A、苯环影响羟基,苯酚具有酸性;
B、乙醛与碳相连的碳上含有H原子,能被还原,乙酸中C上无H原子;
C、苯环影响甲基,使得甲基易氧化;
D、甲基影响苯环,使得甲苯中苯环上的氢原子易被取代.
解答 解:A.苯环影响羟基基,苯酚能跟NaOH溶液反应,而乙醇不能,可说明或原子与原子团间的相互影响会导致物质的化学性质不同,故A不选;
B.乙醛与碳相连的碳上含有H原子,能发生加成反应杯还原,乙酸中C上无H原子,与题给观点无关,故B选;
C.甲基连接在苯环上,可被氧化,说明苯环对甲基影响,故C不选;
D.甲苯与硝酸反应更容易,说明甲基的影响使苯环上的氢变得活泼易被取代,故D不选;
故选:B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、原子或原子团的相互影响为解答的关键,侧重常见有机物结构、性质的考查,题目难度不大.

练习册系列答案
相关题目
19.关于如图图示的说法中正确的是( )
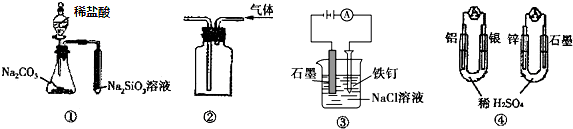

| A. | 用图①所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
| B. | 用图②所示实验装置排空气法收集CH4气体 | |
| C. | 装置③可电解食盐水制氯气 | |
| D. | 图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
20.甲容器中进行如下反应4A(s)+3B(g)?2C(g)+D(g),经2min,B的浓度减少0.6mol/L.对此反应速率的下列说法正确的是( )
| A. | 在2 min末的反应速率,用B表示是 0.3 mol/(L•min) | |
| B. | 用A表示的反应速率是0.4 mol/(L•min) | |
| C. | 若乙容器中也同时进行此反应,且相同时间段内用D表示的速率是0.2 mol/(L•min),则乙容器中反应速率更快 | |
| D. | 对甲容器升高温度,则正反应速率将减小 |
4.某混合气体中可能含有N2、O2、SO2、NO、NO2 中的两种或多种气体.现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色.对于原混合气体成分的判断中正确的是( )
| A. | 肯定有SO2 和NO | B. | 肯定没有N2、O2和NO2 | ||
| C. | 可能有Cl2和O2 | D. | 肯定只有NO |
14.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 在1 mol NaHSO4晶体中,含阳离子数为2NA | |
| B. | 1 mol C4H10分子中共价键总数为13NA | |
| C. | 0.5 mol•L-1 Ba(NO3)2溶液中,NO${\;}_{3}^{-}$的数目为NA | |
| D. | 任何条件下,20 L N2含有的分子数都不可能为NA |
18. 乙醇分子结构中,各种化学键如图所示.乙醇在各种反应中断裂键的说明不正确的是( )
乙醇分子结构中,各种化学键如图所示.乙醇在各种反应中断裂键的说明不正确的是( )
 乙醇分子结构中,各种化学键如图所示.乙醇在各种反应中断裂键的说明不正确的是( )
乙醇分子结构中,各种化学键如图所示.乙醇在各种反应中断裂键的说明不正确的是( )| A. | 在Cu催化下和O2反应时断裂①,③键 | B. | 和金属钠反应时断裂键① | ||
| C. | 完全燃烧时全部断裂 | D. | 与浓H2SO4共热170℃时断裂键②④ |
19.常温下,体积相同,浓度均为0.1mol/L的苯酚钠、碳酸氢钠、碳酸钠、醋酸钠四种溶液pH最大的是( )
| A. | 苯酚钠溶液 | B. | 碳酸氢钠溶液 | C. | 碳酸钠溶液 | D. | 醋酸钠溶液 |
 我国国家标准( GB2760 )规定葡萄酒中SO2最大使用量为0.25g•L-1.某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定.
我国国家标准( GB2760 )规定葡萄酒中SO2最大使用量为0.25g•L-1.某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定.