题目内容
15.已知A~O各代表一种物质,除O外其余物质均由短周期元素组成,它们之间的转化关系如图所示(反应条件略).A、B、H分别是单质.B与冷水缓慢反应,与沸水迅速反应,放出氢气.D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱.C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀.
请回答下列问题:
(1)组成B单质的元素位于周期表第三周期,第ⅡA族.化合物C和D的电子式为
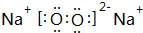 、
、 .
.(2)J的沸点比硒化氢(H2Se)的沸点高,其原因是水分子之间存在氢键且化硒化氢的分子间作用力强.
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O
(4)写出D与足量的N反应生成E和F的化学方程式:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.写出G与F加热反应生成K、I和J的化学方程式:NH4NO3+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaNO3+NH3↑+H2O.
(5)上图中在同一反应里一种物质作氧化剂,又作还原剂,这样的反应共有2个.
分析 B是由短周期元素组成的单质,B与冷水缓慢反应,与沸水迅速反应,放出氢气,可判断B为金属镁.D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反应得到两种碱,可以判断D为氮化镁,所以A为氮气. C为淡黄色固体化合物,可确定C为Na2O2.C与J反应得到G与H,O能与G的水溶液反应生成蓝色沉淀,说明有氢氧化铜生成,则G为NaOH,故J为H2O,H为O2,G与F反应得到K、I与水,且I连续与氧气反应生成M,M与水反应生成L与N,N能与Cu反应生成铜盐,故N为HNO3,则E为Mg(NO3)2,F为NH4NO3,K为NaNO3,I为NH3,故L为NO,M为NO2,O为Cu(NO3)2,据此解答.
解答 解:B是由短周期元素组成的单质,B与冷水缓慢反应,与沸水迅速反应,放出氢气,可判断B为金属镁.D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反应得到两种碱,可以判断D为氮化镁,所以A为氮气. C为淡黄色固体化合物,可确定C为Na2O2.C与J反应得到G与H,O能与G的水溶液反应生成蓝色沉淀,说明有氢氧化铜生成,则G为NaOH,故J为H2O,H为O2,G与F反应得到K、I与水,且I连续与氧气反应生成M,M与水反应生成L与N,N能与Cu反应生成铜盐,故N为HNO3,则E为Mg(NO3)2,F为NH4NO3,K为NaNO3,I为NH3,故L为NO,M为NO2,O为Cu(NO3)2,
(1)组成B单质的元素为Mg元素,原子核外有3个电子层,最外层电子数为2,则应位于周期表第三周期ⅡA族,C为Na2O2,为离子化合物,电子式为 ,D为氮化镁,电子式为
,D为氮化镁,电子式为 ,
,
故答案为:三;ⅡA; ;
; ;
;
(2)J为H2O,水分子之间存在氢键且化硒化氢的分子间作用力强,故其沸点比硒化氢(H2Se)的沸点高,
故答案为:水分子之间存在氢键且化硒化氢的分子间作用力强;
(3)由题意可知,NH3在O2中点燃生成N2和H2O,则反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,
故答案为:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;
(4)D与足量的N反应生成E和F的化学方程式为:Mg3N2+8HNO3=3Mg(NO3)2+2NH4NO3,G与F加热反应生成K、I和J的化学方程式为NH4NO3+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaNO3+NH3↑+H2O,
故答案为:Mg3N2+8HNO3=3Mg(NO3)2+2NH4NO3;NH4NO3+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaNO3+NH3↑+H2O;
(5)上图中,在同一反应里一种物质既作氧化剂,又作还原剂反应有:2Na2O2+2H2O=4NaOH+O2↑,3NO2+H2O=2HNO3+NO,共2个反应,
故答案为:2.
点评 本题考查无机物的推断,题目难度中等,本题中的几个突破口:①B与冷水缓慢反应,与沸水迅速反应,放出氢气,②D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱,③C为淡黄色固体化合物,④蓝色沉淀,再结合转化关系推断,需要学生具备扎实的基础

 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案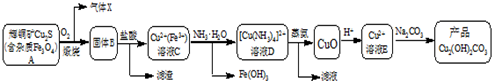
已知:[Cu(NH3)4]2+(aq)═Cu2+(aq)+4NH3(aq)根据以上工艺流程,下列说法不正确的是( )
| A. | 气体X中含有SO2 | |
| B. | 为实现溶液C到溶液D的转化,加NH3•H2O至红棕色沉淀刚好完全,过滤即可 | |
| C. | 蒸氨过程发生总反应的化学方程式为:[Cu(NH3)4]Cl2+H2O$\frac{\underline{\;加热\;}}{\;}$CuO+2HCl↑+4NH3↑ | |
| D. | 在制备产品时,溶液D中不直接加入Na2CO3溶液的原因是游离的Cu2+浓度太低 |
| A. | 在18g18O2中含有NA个氧原子 | |
| B. | 标准状况下,22.4L水中含有2NA个氢原子 | |
| C. | 1mol.L-1NaCl阴离子数为NA | |
| D. | 含NA个Na+的NaOH溶解于lL水中,Na+的物质的量浓度为1mol•L-1 |
| A. | 元素的种类由原子核内质子数决定 | |
| B. | 分子的种类由分子组成决定 | |
| C. | 原子的种类由原子核内中子数决定 | |
| D. | 元素的化学性质由原子最外层电子数决定 |
| A. | 向淀粉碘化钾的溶液中加入氯水,溶液变为蓝色,说明Cl2的氧化性强于I2 | |
| B. | 在高温条件下,C能置换出SiO2中的Si,说明C的氧化性强于Si | |
| C. | 在空气中加热铝箔,发现内部的铝熔化但不滴落,说明铝不易与氧气反应 | |
| D. | 工业上用铝制容器盛装浓硫酸,说明常温下铝和浓硫酸不反应 |
| A. | 原子核内的质子数决定原子种类 | |
| B. | 原子核内的中子数决定核素种类 | |
| C. | 原子核内的中子数决定同位素种类 | |
| D. | 质子数相同的不同核素互称为同位素 |
| A. | 1mol氯气参加反应转移的电子数一定为2NA | |
| B. | 常温下10LpH=13的NaOH溶液中含有的OH-数目约为NA | |
| C. | 将0.1mol氯化铁溶于1L水中,所得溶液含有Fe3+数目为0.1NA | |
| D. | 电解法精炼铜时,当阳极有64g铜溶解,导线上流过电子数目为2NA |
| A. | 乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同 | |
| B. | 溴乙烷与NaOH水溶液共热生成乙烯 | |
| C. | 苯乙烯、聚苯乙烯都能发生加成反应 | |
| D. | 乙酸、乙醛和乙醇三种液体可以用新制氢氧化铜悬浊液鉴别 |
 ,该元素在周期表中的位置为第三周期,第ⅣA族,下列不属于晶体硅的用途的是ACD
,该元素在周期表中的位置为第三周期,第ⅣA族,下列不属于晶体硅的用途的是ACD