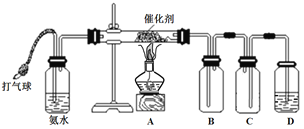
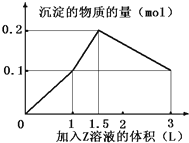
题目内容
【题目】下列变化过程需要加入还原剂才能实现的是
A.H2O2→O2B.SiO2→Si
C.H2SO4(浓)→SO2D.Na2O→NaOH
【答案】B
【解析】
A.H2O2加入MnO2发生分解反应产生O2,不需要加入还原剂就可以实现,A不符合题意;
B.SiO2造高温下被焦炭还原产生单质Si,需加入还原剂才可以实现,B符合题意;
C.S元素化合价降低,可以使用亚硫酸盐与浓硫酸发生复分解反应制取二氧化硫,C不符合题意;
D. Na2O与水反应产生NaOH,各种元素化合价没有发生变化,不属于氧化还原反应,D不符合题意;
故合理选项是B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】用0.001mol/L的酸性高锰酸钾溶液滴定未知浓度的草酸(H2C2O4)溶液,回答下列 问题:
(1)酸性高锰酸钾溶液应该装在下图__________滴定管中。
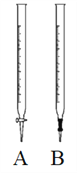
(2)请写出该反应的离子方程式:____________________。
(3)用0.001mol/L的酸性高锰酸钾溶液滴定草酸溶液,滴定终点的判断依据是:_________________。
(4)己知滴定V1ml待测液消耗标准液实验数据如下表
实验次数 | 始读数(ml) | 末读数(ml) | 消耗体积 |
1 | 0.10 | 19.20 | 19.10 |
2 | 1.85 | 20.75 | 18.90 |
3 | 0.00 | 24.06 | 24.06 |
则待测液的浓度为:_______________
(5)滴定结束时,俯视刻度线读取高锰酸钾溶液的体积,会导致测定结果_________(填“偏大”“偏小”或“不影响”)
(6)己知NaHC2O4溶液中草酸氢根离子的电离大于水解,则溶液中各离子的浓度按由大到小的顺序排列的是:_________________________。