题目内容
【题目】按要求填空。
(1)在Fe、Fe2+、Fe3+、H+中,
①只有氧化性的是__;
②只有还原性的是__;
③既有氧化性又有还原性的是__。
(2)已知RxO42-+MnO4-+H+→RO2+Mn2++H2O变化过程中,0.2molRxO42-参加反应,共转移0.4mol电子。
①反应中的被还原的微粒是__。
②x=__。
③参加反应的氢离子的物质的量为__。
【答案】Fe3+、H+ Fe Fe2+ MnO4- 2 0.64mol
【解析】
(1)①微粒中所含元素化合价只能降低不能升高的微粒,只有氧化性;
②微粒中所含元素化合价只能升高不能降低的微粒,只有还原性;
③微粒中所含元素化合价既能升高又能降低的微粒,既有氧化性又有还原性。
(2)①反应中含有化合价降低元素的微粒被还原。
②可建立关系式RxO42-——xRO2,则0.2mol ×(4x-6)= 0.4mol ,由此可求出x。
③将方程式写出并配平,然后利用n(RxO42-)=0.2mol,求出参加反应的氢离子的物质的量。
(1)在Fe、Fe2+、Fe3+、H+中,Fe化合价只能升高不能降低;Fe2+化合价可升高到+3,也可降低到0;Fe3+化合价不能升高,只能降低到+2甚至0;H+化合价只能降低到0,不能升高。
①由以上分析知,只有氧化性的是Fe3+、H+;
②只有还原性的是Fe;
③既有氧化性又有还原性的是Fe2+。答案为:Fe3+、H+; Fe; Fe2+;
(2)在反应RxO42-+MnO4-+H+→RO2+Mn2++H2O中,MnO4-→Mn2+,Mn元素化合价由+7价降低为+2价,则由RxO42-→RO2,R元素的化合价升高。
①反应中被还原的微粒是含有化合价降低元素的反应物,应为MnO4-。
②可建立关系式RxO42-——xRO2,则0.2mol ×(4x-6)= 0.4mol ,求出x=2。
③将方程式写出并配平,即得5R2O42-+2MnO4-+16H+→10RO2+2Mn2++8H2O,n(RxO42-)=0.2mol,则参加反应的氢离子的物质的量为![]() =0.64mol。答案为:MnO4-;2;0.64mol。
=0.64mol。答案为:MnO4-;2;0.64mol。

【题目】下列实验方案中不能达到相应实验目的的是:
A | B | C | D | |
方案 |
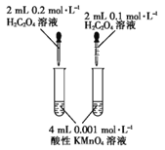
| 在2mL1mol/LNaOH溶液中,加入5滴1mol/L氯化镁溶液,有白色沉淀,再加入5滴氯化铁溶液,观察沉淀颜色 | 实验室制备氢气,用粗锌代替纯锌与稀硫酸反应,反应速率加快 |
|
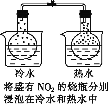
目的 | 探究浓度对化学反应速率的影响 | 探究沉淀溶解平衡的移动 | 探究形成原电池对反应速率的影响 | 探究温度对化学平衡的影响 |
A.AB.BC.CD.D