题目内容
【题目】下列实验方案中不能达到相应实验目的的是:
A | B | C | D | |
方案 |
| 在2mL1mol/LNaOH溶液中,加入5滴1mol/L氯化镁溶液,有白色沉淀,再加入5滴氯化铁溶液,观察沉淀颜色 | 实验室制备氢气,用粗锌代替纯锌与稀硫酸反应,反应速率加快 |
|
目的 | 探究浓度对化学反应速率的影响 | 探究沉淀溶解平衡的移动 | 探究形成原电池对反应速率的影响 | 探究温度对化学平衡的影响 |
A.AB.BC.CD.D
【答案】B
【解析】
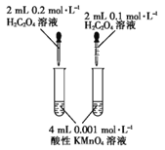
A. 酸性KMnO4溶液等浓度等体积,H2C2O4溶液等体积不同浓度,通过观察紫红色褪去的快慢,探究H2C2O4浓度不同对化学反应速率的影响,能达到目的,A项正确;
B. 在2mL1mol/LNaOH溶液中,加入5滴1mol/L氯化镁溶液,产生白色沉淀,由于NaOH过量,再加入FeCl3时,FeCl3直接与NaOH反应,不能证明沉淀的转化,B项错误;
C. 粗锌与纯锌相比较,粗锌中含有杂质,锌与杂质在稀硫酸中易形成原电池,从而加快了生成氢气的反应速率,快速制取氢气,能达到实验目的,C项正确;
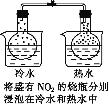
D. 其他条件相同,通过观察温度不同颜色深浅的变化探究温度对化学平衡的影响,D项正确;
答案选B。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目