题目内容
14.粗盐提纯中几次用到玻璃棒,每次使用的作用各是什么?分析 粗盐的提纯中通常用到溶解、过滤、蒸发等步骤来制取精盐,溶解、蒸发时用玻璃棒搅拌,过滤时用玻璃棒引流.
解答 解:在“粗盐提纯”的实验中,操作步骤为溶解-过滤-蒸发,在溶解操作中玻璃棒的作用是搅拌,加快溶解;在过滤操作中玻璃棒的作用是引流;蒸发时玻璃棒的作用是搅拌,防止局部温度过高,造成液滴飞溅,
答:粗盐提纯中3次用到玻璃棒;溶解时作用:搅拌,加快溶解;过滤时作用:引流;蒸发时作用:搅拌,防止液滴飞溅.
点评 本题考查粗盐提纯、物质分离提纯,注意掌握粗盐提纯原理与玻璃棒作用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.海水开发利用的部分过程如图所示.下列说法错误的是( )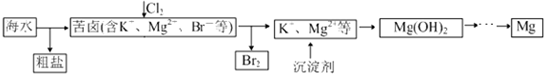

| A. | 粗盐可采用除杂和重结晶等过程提纯 | |
| B. | 向苦卤中通入Cl2 是为了提取溴 | |
| C. | 实际生产中常选用Ca(OH)2作为沉淀剂 | |
| D. | 工业生产中电解熔融氧化镁的方法制取镁 |
5.只用一种试剂就可以鉴别乙酸溶液、葡萄糖溶液、淀粉溶液,这种试剂是( )
| A. | 饱和Na2CO3溶液 | B. | Cu(OH)2悬浊液 | C. | 烧碱溶液 | D. | 碘水 |
9.从如图的溶解度曲线图,可获得的信息是( )


| A. | A、B、C三种物质中A的溶解度最大 | |
| B. | 通过蒸发溶剂的方法可将C从不饱和溶液变成饱和溶液 | |
| C. | 20℃时,100g水中溶解30g A可达到饱和 | |
| D. | 80℃时,100g水不能将50g B溶解完全,而能完全溶解50g C |
19.下列说法正确的是( )
| A. | C11H24、C27H56、C29H60三种物质互为同系物 | |
| B. | C33H68在常温下为液态 | |
| C. | C35H72中氢原子被氯气取代,最多需氯气35mol | |
| D. | 正二十一烷分子中所有碳原子在一条直线上 |
1.研究人员研制利用低品位软锰矿浆(主要成分是MnO2)吸收硫酸厂的尾气SO2,制备硫酸锰的生产流程如下: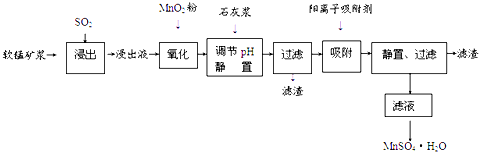
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、
Pb2+等其他金属离子.PbO2的氧化性大于MnO2.
有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见如图.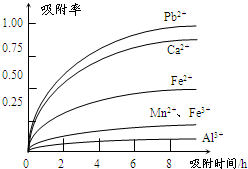
请回答下列问题:
(1)写出浸出过程中生成Mn2+反应的化学方程式SO2+MnO2=MnSO4,
(2)氧化过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至4.7≤pH<8.3范围.
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子半径、金属离子电荷等.吸附步骤除去的主要离子为:Pb2+、Ca2+.
(5)电解MnSO4和ZnSO4的混合溶液可制备MnO2和Zn,写出阳极的电极反应方程式Mn2+-2e-+2H2O=MnO2↓+4H+.

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、
Pb2+等其他金属离子.PbO2的氧化性大于MnO2.
有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见如图.

| 离子 | 离子半径(pm) | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
(1)写出浸出过程中生成Mn2+反应的化学方程式SO2+MnO2=MnSO4,
(2)氧化过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至4.7≤pH<8.3范围.
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子半径、金属离子电荷等.吸附步骤除去的主要离子为:Pb2+、Ca2+.
(5)电解MnSO4和ZnSO4的混合溶液可制备MnO2和Zn,写出阳极的电极反应方程式Mn2+-2e-+2H2O=MnO2↓+4H+.
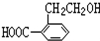 .
.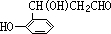 ;
;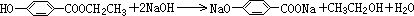 .
.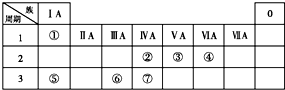 下表为元素周期表的一部分,请参照①~⑦相关元素在表中的位置,用化学用语回答下列问题:
下表为元素周期表的一部分,请参照①~⑦相关元素在表中的位置,用化学用语回答下列问题: