题目内容
10.有关如图装置中的叙述正确的是( )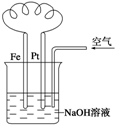
| A. | 这是电解NaOH溶液的装置 | |
| B. | 这是吸氧腐蚀的原电池装置 | |
| C. | Fe为正极,电极反应为:Fe-2e-+2OH-═Fe(OH)2 | |
| D. | NaOH溶液的碱性逐渐减弱 |
分析 碱性条件下,铁、铂丝和含有空气的氢氧化钠溶液构成原电池,铁发生吸氧腐蚀,铁作负极,负极上铁失电子发生氧化反应,铂丝作正极,正极上氧气得电子发生还原反应.
解答 解:A.该装置符合原电池的构成条件,所以属于原电池,发生铁的吸氧腐蚀,故A错误;
B.该装置符合原电池的构成条件,所以属于原电池,发生铁的吸氧腐蚀,负极上电极反应式为Fe-2e-═Fe2+,正极上的电极反应式为:O2+2H2O+4e-═4OH-,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定易被氧化生成氢氧化铁,反应方程式为:4Fe(OH)2+2H2O+O2═4Fe(OH)3,故B正确;
C.铁作负极,电极反应式为Fe-2e-═Fe2+,故C错误;
D.负极反应式为2Fe═2Fe2++4e-,正极上的反应式为:2H2O+O2+4e-═40H-,所以总反应为2Fe+2H2O+O2═2Fe(OH)2,根据电池反应式知,电解质溶液中氢氧根离子浓度不变,故D错误;
故选:B.
点评 本题考查了铁的吸氧腐蚀,明确原电池原理是解本题关键,根据正负极上得失电子及反应类型来分析解答,难点是电极反应式的书写.

练习册系列答案
相关题目
20.下列变化过程中需要吸收能量的是( )
| A. | 2H2+O2═2H2O | B. | H2→2H | C. | CaO+H2O═Ca(OH)2 | D. | H++OH-=H2O |
1.下列反应的离子方程式书写正确的是( )
| A. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 氢氧化钡溶液与稀 H2SO4:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| C. | 向氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | 钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ |
18.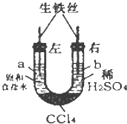 利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间.下列说法不正确的是( )
利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间.下列说法不正确的是( )
 利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间.下列说法不正确的是( )
利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间.下列说法不正确的是( )| A. | a处溶液的pH增大,b处溶液的pH减小 | |
| B. | 一段时间后,a管液面高于b管液面 | |
| C. | a管发生吸氧腐蚀,b管发生析氧腐蚀 | |
| D. | a、b两处具有相同的电极反应式:Fe-2e-=Fe2+ |
5.将一定量的Na、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到a L混合气体.将该混合气体通过电火花引燃,恰好完全反应,则原混合物中Na、Na2O、Na2O2的物质的量之比可能为( )
| A. | 2:1:1 | B. | 1:1:2 | C. | 1:2:1 | D. | 4:3:3 |
15. W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,其最外层电子数之和等于24,由此可知下列说法错误的是( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,其最外层电子数之和等于24,由此可知下列说法错误的是( )
 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,其最外层电子数之和等于24,由此可知下列说法错误的是( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,其最外层电子数之和等于24,由此可知下列说法错误的是( )| A. | 原子半径大小:W>X | B. | 气态氢化物的沸点:Y>X | ||
| C. | 简单阴离子的还原性:Y>Z | D. | 气态氢化物的稳定性:X>Y |
19.下列反应属于氮的固定的是( )
| A. | NH4Cl与Ca(OH)2反应生成NH3 | B. | 空气在雷电作用下所产生NO | ||
| C. | NO和O2生成NO2 | D. | 铜与浓硝酸反应产生NO2 |
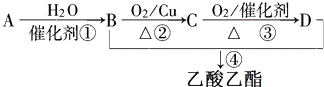
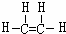 .
.

 .
. .
.