题目内容
1.下列反应的离子方程式书写正确的是( )| A. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 氢氧化钡溶液与稀 H2SO4:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| C. | 向氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | 钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ |
分析 A.一水合氨为弱电解质,离子方程式中不能拆开;
B.氢离子、氢氧根离子的系数与硫酸、氢氧化钡的化学式组成不相符;
C.氯化亚铁与氯气反应生成氯化铁;
D.离子方程式两边正电荷不相等,违反了电荷守恒.
解答 解:A.AlCl3溶液中加入足量的氨水,反应生成氢氧化铝沉淀,一水合氨应该保留分子式,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故A错误;
B.氢氧化钡溶液与稀H2SO4,反应生成硫酸钡沉淀和水,正确的离子方程式为:Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O,故B错误;
C.向氯化亚铁溶液中通入氯气,反应生成氯化铁,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,故C正确;
D.钠和冷水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,为中等难度的试题,注意掌握离子方程式正误判断常用方法,如:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
11.2007年3月21日,我国公布了111号元素Rg的中文名称.该元素名称及所在周期是( )
| A. | 钅仑 第七周期 | B. | 镭 第七周期 | C. | 铼 第六周期 | D. | 氡 第六周期 |
12.下列有关叙述中错误的是( )
| A. | 元素的性质随着核电荷数的递增而呈周期性变化 | |
| B. | 原子的原子核都是由质子和中子构成的 | |
| C. | 两个原子如果核外电子排布相同,一定是同一种元素 | |
| D. | 原子的次外层电子数不一定是8个 |
9.将甲烷与氯气按物质的量之比1:3混合,光照条件下发生化学反应后,得到的有机产物是( )
①CH3Cl ②CH2Cl2 ③CHCl3 ④CCl4.
①CH3Cl ②CH2Cl2 ③CHCl3 ④CCl4.
| A. | 只有① | B. | 只有③ | C. | ①②③的混合物 | D. | ①②③④的混合物 |
16.以下物质间的每步转化都可以通过一步反应能实现的是( )
| A. | Al→Al2O3→Al(OH)3→Na[Al(OH)4] | B. | Fe→FeO→Fe(OH)2→Fe(OH)3 | ||
| C. | Si→SiO2→H2SiO3→Na2SiO3 | D. | Na→Na2O2→Na2CO3→NaOH |
10.有关如图装置中的叙述正确的是( )
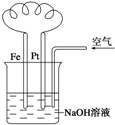

| A. | 这是电解NaOH溶液的装置 | |
| B. | 这是吸氧腐蚀的原电池装置 | |
| C. | Fe为正极,电极反应为:Fe-2e-+2OH-═Fe(OH)2 | |
| D. | NaOH溶液的碱性逐渐减弱 |
11.下列有关金属的说法正确的是( )
| A. | 金属单质在常温下都是固体 | |
| B. | 金属原子只有还原性,金属阳离子只有氧化性 | |
| C. | 含金属元素的离子都是阳离子 | |
| D. | 金属阳离子被还原不一定生成金属单质 |