题目内容
【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
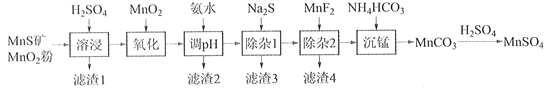
相关金属离子[c0(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________。
(2)“氧化”中添加适量的MnO2的作用是将________________________。
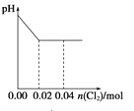
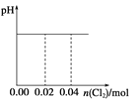
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_____________________________________________________________________。
(6)写出“沉锰”的离子方程式___________________________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnz2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___________。
时,z=___________。
【答案】SiO2(不溶性硅酸盐) MnO2+MnS+2H2SO4=2MnSO4+S+2H2O 将Fe2+氧化为Fe3+ 4.7 NiS和ZnS F与H+结合形成弱电解质HF,MgF2![]() Mg2++2F平衡向右移动 Mn2++2
Mg2++2F平衡向右移动 Mn2++2![]() =MnCO3↓+CO2↑+H2O
=MnCO3↓+CO2↑+H2O ![]()
【解析】
(1)Si元素以SiO2或不溶性硅盐存在,SiO2与硫酸不反应,所以滤渣I中除了S还有SiO2;在硫酸的溶浸过程中,二氧化锰和硫化锰发生了氧化还原反应,二氧化锰作氧化剂,硫化锰作还原剂,方程式为:MnO2+MnS+2H2SO4=2MnSO4+S+2H2O;
(2)二氧化锰作为氧化剂,使得MnS反应完全,且将溶液中Fe2+氧化为Fe3+;
(3)由表中数据知pH在4.7时,Fe3+和Al3+沉淀完全,所以应该控制pH在4.7~6之间;
(4)根据题干信息,加入Na2S除杂为了除去锌离子和镍离子,所以滤渣3是生成的沉淀ZnS和NiS;
(5)由HF![]() H++F-知,酸度过大,F-浓度减低,使得MgF2
H++F-知,酸度过大,F-浓度减低,使得MgF2![]() Mg2++2F-平衡向沉淀溶解方向移动,Mg2+沉淀不完全;
Mg2++2F-平衡向沉淀溶解方向移动,Mg2+沉淀不完全;
(6)根据题干信息沉锰的过程是生成了MnCO3沉淀,所以反应离子方程式为:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O;
(7)根据化合物中各元素化合价代数和为0的规律得:1+2x+3y+4z=6,已知,x=y=1/3,带入计算得:z=1/3

【题目】乙醇是制取饮料、香精、染料、涂料、洗涤剂等产品的原料.
完成下列填空:
(1)实验室用乙醇制取乙烯时,浓硫酸的用量远远超过作为催化剂的正常用量,原因是______.
(2)验证乙烯加成反应性质时,需对乙烯气体中的干扰物质进行处理,可选用的试剂是______(填写化学式);能确定乙烯通入溴水中发生了加成反应的事实是______.(选填编号)
a.溴水褪色 b.有油状物质生成
c.反应后水溶液酸性增强 d.反应后水溶液接近中性
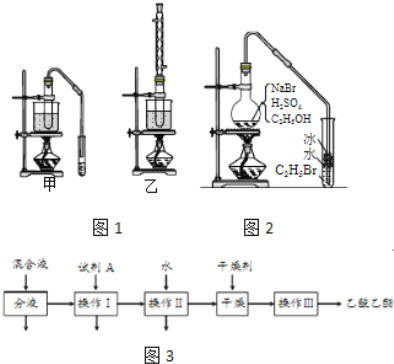
(3)实验室用乙醇和乙酸制备乙酸乙酯时,甲乙两套装置如图1都可以选用.关于这两套装置的说法正确的是______.(选填编号)
物质 | 沸点(℃) |
乙醇 | 78.5 |
乙酸 | 117.9 |
乙酸乙酯 | 77 |
a.甲装置乙酸转化率高 b.乙装置乙酸转化率高
c.甲装置有冷凝回流措施 d.乙装置有冷凝回流措施
(4)用乙装置实验时,提纯乙中乙酸乙酯的流程如图3,以上流程中试剂A的化学式是______;操作Ⅱ的名称是______;操作Ⅲ一般适用于分离______混合物.
(5)如图2是用乙醇制备溴乙烷的装置,实验中有两种加料方案:
①先加溴化钠→再加乙醇→最后加1:1浓硫酸;
②先加溴化钠→再加1:1浓硫酸→最后加乙醇.
按方案①和②实验时,产物都有明显颜色,若在试管中加入______,产物可变为无色.与方案①相比较,方案②的明显缺点是______.