题目内容
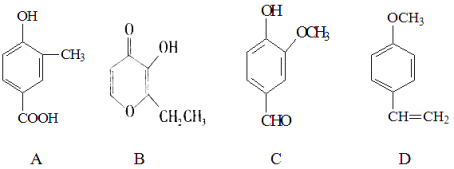
【题目】下列关于有机物![]() 的叙述不正确的是( )
的叙述不正确的是( )
A.该物质在一定的条件下能形成高分子化合物
B.分子中最多有15个原子位于同一平面内
C.1mol该有机物可与4 molH2发生加成反应
D.该物质能使溴水褪色
【答案】B
【解析】
A. 有机物结构中存在碳碳双键,可发生加聚反应而形成高分子化合物,A项正确;
B. 与双键直接相连的原子共面,苯环具有平面结构,因此与苯环和碳碳双键直接相连的原子在同一平面上,则分子中最多有17个原子位于同一平面内,B项错误;
C. 1mol碳碳双键和1molH2加成,1mol苯环可以与3mol氢气发生加成反应,因而1mol该有机物可与4 molH2发生加成反应,C项正确;
D. 碳碳双键可以与溴水发生加成反应而使溴水褪色,D项正确;
答案选B。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案【题目】铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如图:
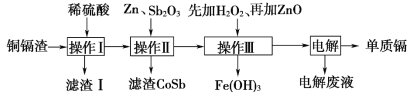
表中列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol·L-1)
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)酸浸时粉碎铜镉渣的目的是___。
(2)操作Ⅰ产生的滤渣主要成分为__(填化学式)。
(3)①操作Ⅲ中先加入适量H2O2,发生反应的离子方程式为__。
②再加入ZnO控制反应液的pH,pH范围为__,判断依据是__。
③若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。请设计实验方案加以鉴别:__。
(4)处理含镉废水常用加入碳酸钙实现沉淀转化,该沉淀转化的反应方程式为___。除去工业废水中的Cd2+时,若反应达到平衡后溶液中c(Ca2+)=0.1mol·L-1,溶液中c(Cd2+)=__mol·L-1[已知25℃,Ksp(CdCO3)=5.6×10-12,Ksp(CaCO3)=2.8×10-9]。