��Ŀ����
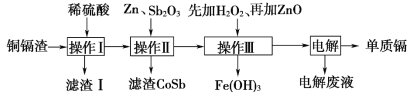
����Ŀ��ͭ������Ҫ��п��ͭ��������(Cd)����(Co)�ȵ��ʡ�ʪ����п������ͭ�����������������ӵĹ���������ͼ��
�����г�����ؽ������������������������pH(�������ӵ���ʼŨ��Ϊ0.1mol��L-1)
�������� | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
��ʼ������pH | 1.5 | 6.5 | 7.2 |
������ȫ��pH | 3.3 | 9.9 | 9.5 |
��1�����ʱ����ͭ������Ŀ����___��
��2�������������������Ҫ�ɷ�Ϊ__(�ѧʽ)��
��3���ٲ��������ȼ�������H2O2��������Ӧ�����ӷ���ʽΪ__��
���ټ���ZnO���Ʒ�ӦҺ��pH��pH��ΧΪ__���ж�������__��
���������H2O2���㣬����ZnO�����õĵ��Һ�лẬ��FeԪ�ء������ʵ�鷽�����Լ���__��
��4���������ӷ�ˮ���ü���̼���ʵ�ֳ���ת�����ó���ת���ķ�Ӧ����ʽΪ___����ȥ��ҵ��ˮ�е�Cd2+ʱ������Ӧ�ﵽƽ�����Һ��c(Ca2+)=0.1mol��L-1����Һ��c(Cd2+)=__mol��L-1[��֪25�棬Ksp(CdCO3)=5.6��10-12��Ksp(CaCO3)=2.8��10-9]��
���𰸡���������ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵĽ����� Cu 2Fe2++H2O2+2H+=2Fe3++2H2O 3.3��pH��7.2 ���ݱ����е���Ϣ��֪��3.3��pH��7.2ʱ����ȷ��Fe3+������ȫ����Cd2+������� ȡ���Һ�������Թ��У������еμӼ���KSCN��Һ���ٵ���H2O2��Һ������Һ��죨�������еμ�K3[Fe(CN)6]��Һ��������ɫ������������Һ�к���FeԪ�� CaCO3(s)+Cd2+(aq)![]() CdCO3(s)+Ca2+(aq) 2.0��10-4
CdCO3(s)+Ca2+(aq) 2.0��10-4
��������
��ʪ����п������ͭ�������������ӵ����̣�ͭ������Ҫ��п��ͭ�������ӣ�Cd�����ܣ�Co���ȵ��ʣ�����ϡ���ᣬͭ���ܣ�����I���ˣ���Һ����Zn2����Fe2����Cd2����Zn2����Co2��������Һ����п�����Sb2O3��п�ۻ���Sb2O3���γ���ز����Ͻ�CoSb��ȥ�ܣ���������ˣ�����ܺ����Һ�м���H2O2��Һ����Fe2��ΪFe3������������п����pHʹFe3��������������˳�ȥ����⺬��Zn2����Co2������Һ���ɵ��ӵ��ʡ�
��1�����ʱ����ͭ������Ŀ��������������ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵĽ����ʣ��ʴ�Ϊ����������ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵĽ����ʣ�
��2��ͭ��ϡ�����Ӧ�������������������Ҫ�ɷ�ΪCu���ʴ�Ϊ��Cu��
��3����˫��ˮ���������ԣ��ܰ�������������Ϊ�����ӣ����������ȼ�������H2O2��������Ӧ�����ӷ���ʽΪ2Fe2��+H2O2+2H��=2Fe3��+2H2O���ʴ�Ϊ��2Fe2��+H2O2+2H��=2Fe3��+2H2O��
���ټ���ZnO���Ʒ�ӦҺ��pH�����ݱ����е���Ϣ��֪��3.3��pH��7.2ʱ����ȷ��Fe3��������ȫ����Cd2��������������pH��ΧΪ3.3��pH��7.2���ʴ�Ϊ��3.3��pH��7.2�����ݱ����е���Ϣ��֪��3.3��pH��7.2ʱ����ȷ��Fe3��������ȫ����Cd2�����������
���������H2O2���㣬����ZnO�����õĵ��Һ�лẬ��FeԪ�ء��������Һ�����������Ӳ��࣬�����������Ӽ��ɡ�����Ϊ��ȡ���Һ�������Թ��У������еμӼ���KSCN��Һ���ٵ���H2O2��Һ������Һ��죨�������еμ�K3[Fe(CN)6]��Һ��������ɫ������������Һ�к���FeԪ�أ��ʴ�Ϊ��ȡ���Һ�������Թ��У������еμӼ���KSCN��Һ���ٵ���H2O2��Һ������Һ��죨�������еμ�K3[Fe(CN)6]��Һ��������ɫ������������Һ�к���FeԪ�أ�
��4�������ܶȻ�������С��֪KspԽС���ܽ��ԽС������Խ��ȫ���������ӷ�ˮ���ü���̼���ʵ�ֳ���ת�����ó���ת���ķ�Ӧ����ʽΪCaCO3(s)+Cd2+(aq)![]() CdCO3(s)+Ca2+(aq)����ȥ��ҵ��ˮ�е�Cd2+ʱ������Ӧ�ﵽƽ�����Һ��c(Ca2+)=0.1mol��L-1��Ksp(CaCO3)=c(Ca2+)��c(CO
CdCO3(s)+Ca2+(aq)����ȥ��ҵ��ˮ�е�Cd2+ʱ������Ӧ�ﵽƽ�����Һ��c(Ca2+)=0.1mol��L-1��Ksp(CaCO3)=c(Ca2+)��c(CO![]() )=2.8��10-9����֪��Һ��̼���Ũ����2.8��10-8mol��L��1���ٸ���Ksp(CdCO3)=c(Cd2+)��c(CO
)=2.8��10-9����֪��Һ��̼���Ũ����2.8��10-8mol��L��1���ٸ���Ksp(CdCO3)=c(Cd2+)��c(CO![]() )=5.6��10-12����֪c��Cd2����=2.0��10-4mol��L-1���ʴ�Ϊ��CaCO3(s)+Cd2+(aq)
)=5.6��10-12����֪c��Cd2����=2.0��10-4mol��L-1���ʴ�Ϊ��CaCO3(s)+Cd2+(aq)![]() CdCO3(s)+Ca2+(aq)��2.0��10-4��
CdCO3(s)+Ca2+(aq)��2.0��10-4��

 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д�