题目内容
【题目】根据所学知识完成题目:
(1)下列物质含有离子键的是
A.H2
B.CO2
C.NH3
D.NaOH
(2)下列物质中含有共价键的离子化合物是
A.H2O
B.CaCl2
C.NH4Cl
D.HCl
(3)NaCl、NH3的电子式 .
【答案】
(1)D
(2)C
(3)![]()
【解析】解:(1)N2属于单质分子,分子中只有共价键;CO2、NH3分子中只有共价键;NaOH中钠离子和氢氧根离子之间存在离子键、O原子和H原子之间存在共价键,所以答案是:D;(2)A.H2O中只含共价键,为共价化合物,故A错误;B.CaCl2中只含离子键,不含共价键,属于离子化合物,故B错误;C.NH4Cl中铵根离子和氯离子之间存在离子键,氮原子和氢原子之间存在共价键,氯离子中氮原子和氧原子之间存在共价键,故C正确;D.HCl中只含共价键,为共价化合物,故D错误.所以答案是:C;(3)氯化钠是离子化合物,是钠离子和氯离子通过静电作用形成的,其电子式为 ![]() ;氨气为共价化合物,分子中存在3对共用电子对,氮原子最外层达到8个电子,氢原子最外层达到2个电子,氨气分子的电子式为
;氨气为共价化合物,分子中存在3对共用电子对,氮原子最外层达到8个电子,氢原子最外层达到2个电子,氨气分子的电子式为 ![]() ,所以答案是:
,所以答案是: ![]() ;
; ![]() .
.
【考点精析】本题主要考查了离子键的相关知识点,需要掌握成键元素:活泼金属(或NH4+)与活泼的非金属(或酸根,OH-);静电作用:指静电吸引和静电排斥的平衡才能正确解答此题.

【题目】甲醇合成反应及其能量变化如图a所示: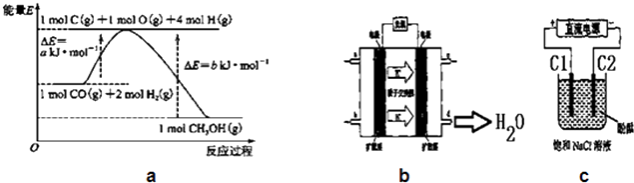
(1)写出合成甲醇的热化学方程式 .
(2)实验室在1L的密闭容器中进行模拟合成实验.将1mol CO和2molH2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的浓度如下表所示:
时间浓度(mol/L)温度 | 10min | 20min | 30min | 40min | 50min | 60min |
300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
在300℃反应开始10min内,H2的平均反应速率为v(H2)= .
(3)在500℃达到平衡时,平衡常数K= .
(4)在另一体积不变的密闭容器中,充入1.2mol CO和2.0mol H2 , 一定条件下达到平衡,测得容器中压强为起始压强的一半.计算该条件下H2的转化率为 .
(5)铜基催化剂具有活性高、选择性好和条件温和的特点,已广泛地使用于CO/CO2的加氢合成甲醇.使用铜基催化剂后,该反应中a的大小变化对反应热△H有无影响, . (填“有影响”或“无影响”)
(6)2009年,长春应用化学研究所在甲醇燃料电池技术上获得新突破,原理如图b所示.请写出从C口通入O2发生的电极反应式 .
(7)用上述电池做电源,用图c装置电解饱和食盐水(C1、C2均为石墨电极).①该反应的离子方程式 .
②电解开始后在电极的周围(填“C1”或“C2”)先出现红色.



