题目内容
【题目】请回答下列问题:
(1)羰基铁[Fe(CO)5]会使合成甲醇和合成氨等生产过程中的催化剂中毒.Fe(CO)5常温下呈液态,熔点为﹣20.5℃,沸点为103℃,易溶于非极性溶剂.据此可以判断Fe(CO)5晶体类型为__。
(2)科学家通过X射线探明,MgO、CaO的晶体结构与NaCl晶体结构相似(如图所示)
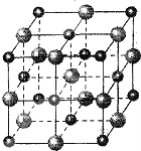
①比较晶体熔点的高低MgO__CaO(填“高于”或“低于”),
②Mg2+的配位原子所构成的立体几何构型为__,③MgCO3晶格能大于CaCO3,为何MgCO3更易分解__。
(3)Ni的堆积与MgO中氧原子堆积相同,Ni可以吸附H2,氢以单个原子形式填入四面体空隙,则Ni最大量吸收H2后,n(Ni):n(H)=__。
【答案】分子晶体 高于 正八面体 氧化镁的晶格能比氧化钙的晶格能大 1:2
【解析】
(1)根据晶体的性质,常温下为液体,熔沸点低来分析;
(2) ①离子晶体中,离子半径小的晶格能大,熔点高;
②该体系为镁离子,六个面的面心为配位原子;
③分解生成金属氧化物,利用氧化物的晶格能来分析;
(3)Ni的堆积与MgO中氧原子堆积相同,晶胞中Ni为1+12×1/4=4,Ni可以吸附H2,氢以单个原子形式填入四面体空隙,则一个晶胞中有8个H。
(1)由晶体具有常温下为液体,熔沸点低的性质可以知道,该晶体为分子晶体;因此,本题正确答案是:分子晶体;
(2)①离子晶体中,因镁离子半径小,则晶格能大,所以氧化镁的熔点高于氧化钙的熔点;因此,本题正确答案是:高于;
②该体系为镁离子,六个面的面心为配位原子,则形成空间正八面体结构;因此,本题正确答案是:正八面体;
③碳酸盐分解生成金属氧化物,因镁离子的半径比钙离子的半径小,则氧化镁的晶格能比氧化钙的晶格能大,所以MgCO3更易分解;
因此,本题正确答案是:氧化镁的晶格能比氧化钙的晶格能大;
(3)Ni的堆积与MgO中氧原子堆积相同,O原子占据体心和棱心,晶胞中Ni为1+12×1/4=4,Ni可以吸附H2,氢以单个原子形式填入四面体空隙,由图可以知道有8个四面体,则一个晶胞中有8个H,所以Ni最大量吸收H2后,n(Ni):n(H)=4:8=1:2;因此,本题正确答案是:1:2。

【题目】硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3、MgO、CaO等,生产工艺流程图如下:

(1)将菱锌矿研磨成粉的目的是___________________________。
(2)写出Fe3+水解的离子方程式_____________________________________________。
(3)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为__________。
沉淀化学式 | Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 |
开始沉淀的pH | 10.4 | 6.4 |
|
|
沉淀完全的pH | 12.4 | 8.0 |
|
|
开始溶解的pH |
| 10.5 |
|
|
Ksp | 5.6×10-12 |
| 6.8×10-6 | 2.8×10-9 |
(4)工业上从“滤液3”制取MgO过程中,合适的反应物是________选填序号。
A、大理石粉 B、石灰乳 C、纯碱溶液 D、氨水
(5)“滤液4”之后的操作依次为______________、______________、过滤、洗涤、干燥。
(6)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于__________用代数式表示。